修回日期: 2026-02-23
接受日期: 2026-02-25
在线出版日期: 2026-02-28
幽门螺旋杆菌(Helicobacter pylori, H. pylori)慢性感染与代谢功能障碍相关脂肪性肝病(metabolic dysfunction-associated fatty liver disease, MAFLD)之间的联系引起了学术界关注, 本研究旨在探讨H. pylori感染、脂质代谢和肝酶谱在MAFLD中的作用.
调查H. pylori感染与MAFLD风险之间的关系, 并定量评估脂代谢标志物和肝功能指标的中介作用.
使用美国国家健康和营养检查调查的横断面数据, 包括4455名成年参与者. 多变量逻辑回归用于分析H. pylori感染(分类和连续ISR)和MAFLD风险之间的关系, 限制性立方样条用于检查剂量反应关系. 使用非参数bootstrap方法(1000个重样本)进行中介分析, 以量化血脂和肝功能指标的间接影响. 所有模型都根据协变量进行了调整, 包括年龄、性别、吸烟、饮酒和糖尿病.
H. pylori感染与MAFLD风险增加显著相关[感染与非感染: 比值比(odd ratio, OR) = 1.15, 95%置信区间(confidence interval, CI): 1.00-1.32; ISR连续: OR = 1.10, 95%CI: 1.03-1.17]. 中介分析显示, 低密度脂蛋白胆固醇(中介比例22.03%-22.99%)和高密度脂蛋白胆固醇(中介比例30.61%-31.09%)是主要的中介. 包括碱性磷酸酶(中介比例4.47%-8.18%)、白蛋白(中介比例11.39%-18.77%)和γ-谷氨酰转移酶(中介比例2.02%-3.48%)在内的几个肝功能指标也显示出显著的介导效应. 亚组分析表明, 性别、糖尿病、吸烟、饮酒或身体质量指数对疗效没有显著影响.
H. pylori感染是MAFLD的独立危险因素, 其作用部分通过血脂异常和某些肝功能指标的改变介导. 这些发现强调了在MAFLD治疗中考虑慢性感染的重要性, 并为进一步探索潜在的代谢途径提供了流行病学证据.
核心提要: 幽门螺杆菌(Helicobacter pylori, H. pylori)感染与代谢功能障碍相关脂肪性肝病(metabolic dysfunction-associated fatty liver disease, MAFLD)风险增加显著相关; 低密度脂蛋白胆固醇和高密度脂蛋白胆固醇是主要的中介. 包括碱性磷酸酶、白蛋白和γ-谷氨酰转移酶在内的几个肝功能指标也显示出显著的介导效应. H. pylori感染是MAFLD的独立危险因素, 其作用部分通过血脂异常和某些肝功能指标的改变介导.
引文著录: 孙延成, 李妍, 李中正, 刘一品. 幽门螺杆菌感染、脂质代谢和肝酶谱在代谢相关脂肪性肝病中的作用: 基于NHANES的中介分析. 世界华人消化杂志 2026; 34(2): 138-150
Revised: February 23, 2026
Accepted: February 25, 2026
Published online: February 28, 2026
The relationship between chronic Helicobacter pylori (H. pylori) infection and metabolic dysfunction-associated fatty liver disease (MAFLD) has attracted academic attention. The purpose of this study was to explore the role of H. pylori, lipid metabolism, and liver function in MAFLD.
To investigate the association between H. pylori infection and the risk of MAFLD, and to quantitatively evaluate the mediating effects of lipid metabolism markers and liver function indicators.
Using cross-sectional data from the National Health and Nutrition Examination Survey, 4455 adult participants were included. Multivariable logistic regression was used to analyze the association between H. pylori infection [categorical and continuous index signal ratio (ISR)] and MAFLD risk, and restricted cubic splines were applied to examine dose-response relationships. Mediation analysis was performed using the nonparametric bootstrap method (1000 resamples) to quantify the indirect effects of lipid and liver function indicators. All models were adjusted for covariates including age, sex, smoking, alcohol use, and diabetes.
H. pylori infection was significantly associated with an increased risk of MAFLD [infected vs non-infected: Odds ratio (OR) = 1.15, 95% confidence interval (CI): 1.00-1.32; continuous ISR: OR = 1.10, 95%CI: 1.03-1.17]. Mediation analysis revealed that non-high-density lipoprotein (HDL) cholesterol (proportion mediated: 22.03%-22.99%) and HDL cholesterol (proportion mediated: 30.61%-31.09%) were the primary mediators. Several liver function indicators, including alkaline phosphatase (proportion mediated: 4.47%-8.18%), albumin (11.39%-18.77%), and gamma-glutamyl transferase (2.02%-3.48%), also showed significant mediating effects. Subgroup analyses indicated no significant effect modification by sex, diabetes, smoking, alcohol use, or body mass index.
H. pylori infection is an independent risk factor for MAFLD, and its effect is partially mediated through dyslipidemia and alterations in certain liver function indicators. These findings highlight the importance of considering chronic infection in MAFLD management and provide epidemiological evidence for further exploration of underlying metabolic pathways.
- Citation: Sun YC, Li Y, Li ZZ, Liu YP. Role of Helicobacter pylori infection, lipid metabolism, and liver function markers in metabolic dysfunction-associated fatty liver disease: A mediation analysis based on NHANES. Shijie Huaren Xiaohua Zazhi 2026; 34(2): 138-150
- URL: https://www.wjgnet.com/1009-3079/full/v34/i2/138.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v34.i2.138
代谢功能障碍相关脂肪性肝病(metabolic dysfunction-associated fatty liver disease, MAFLD)是世界上最常见的慢性肝病. 在过去的几十年里, 患病率持续上升, 成为一个主要的公共卫生挑战[1]. 据估计, 全球约有25%-30%的成年人受其影响, 其中中国患病率接近30%, 超过病毒性肝炎, 成为慢性肝病的首要原因[2]. MAFLD是肝脏系统性代谢功能障碍的一种表现. 它与肥胖、2型糖尿病、血脂异常、心血管疾病等多种代谢并发症密切相关, 严重影响患者的长期生活质量和预后[3]. 这反映了其发生发展与全身代谢状态密切相关.
除了经典的代谢危险因素外, 慢性感染和炎症状态的作用越来越受到关注. 幽门螺杆菌(Helicobacter pylori, H. pylori)作为一种革兰氏阴性杆菌, 全球感染率高, 不仅是慢性胃炎、消化性溃疡和胃癌的主要原因, 而且其引起的持续、低度全身炎症反应可能对器官的代谢稳态产生深远影响[4]. 近年来, 越来越多的流行病学证据表明, H. pylori感染可能与代谢功能障碍有关, 如肥胖、胰岛素抵抗、血脂异常以及2型糖尿病等[5-7]. 因此, H. pylori感染也可能是MAFLD发病的潜在危险因素. 其原因可能是与诱导全身低度炎症、影响胃肠激素分泌、干扰肠道微生物群稳态和胆汁酸代谢等多种途径影响肝脏代谢[8-10].
因此, 我们利用2017-2018年国家健康与营养调查(National Health and Nutrition Examination Survey, NHANES)数据并采用结合中介分析的横断面设计来评估H. pylori感染、脂质代谢和肝酶谱在代谢相关脂肪性肝病中的作用.
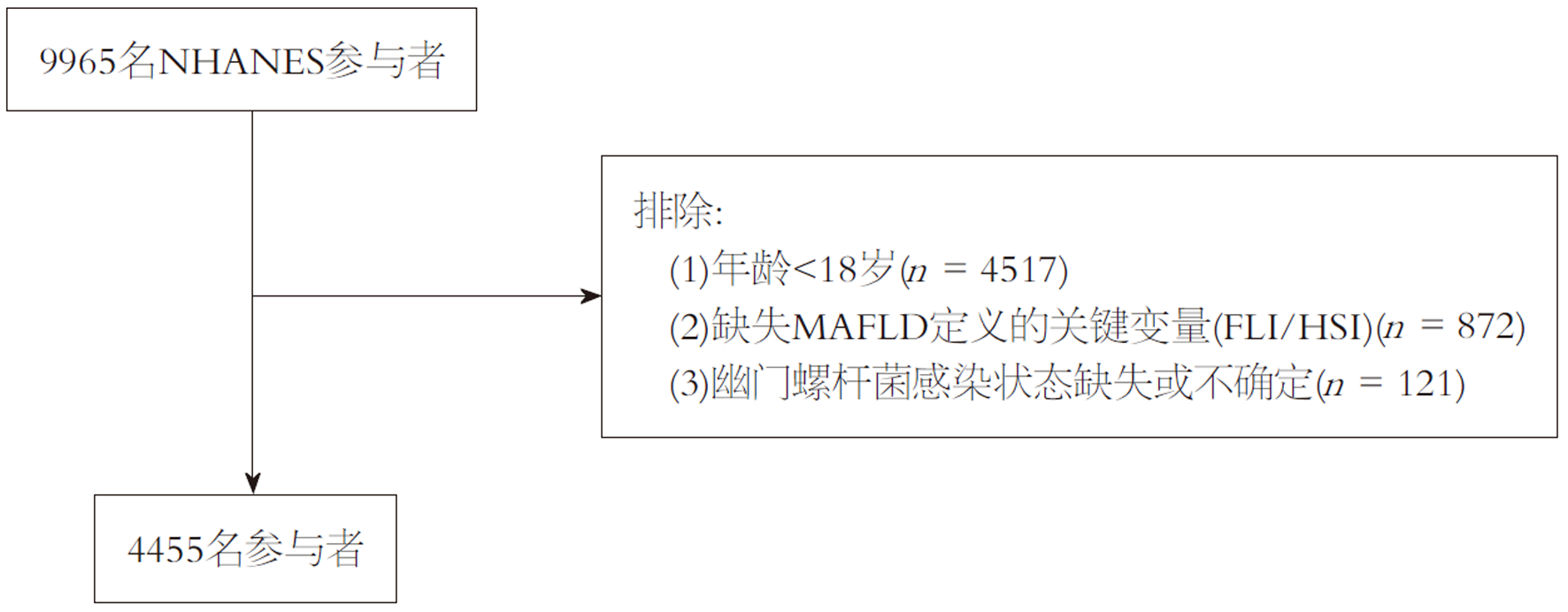
研究人群: 使用NHANES数据库数据. 通过年龄、检测数据是否完整、感染是否明确等多阶段严格纳排标准筛选后, 共有4455名符合标准的参与者被纳入分析. 筛选过程如图1所示.
H. pylori感染判定: 通过酶联免疫吸附试验测定的ISR(指数信号比)值评估H. pylori感染状态以及反映血清中H. pylori IgG抗体的水平. 本研究仅包括H. pylori抗体阴性(ISR<0.9)和H. pylori抗体阳性(ISR>1.1)的受试者, 为避免误导统计结果, 分析中排除了模糊值(0.9≤ISR≤1.1).
1.2.1 MAFLD诊断: MAFLD基于2020年国际专家共识, 要求同时满足以下两个条件: (1)肝脂肪变性; (2)以下三种代谢异常中的至少一种: 超重/肥胖, 2型糖尿病或至少两种代谢异常. 使用非侵入性指标评估肝脏脂肪变性: 肝脏脂肪变性指数(hepatic steatosis index, HSI)或脂肪肝指数(fatty liver index, FLI). 将肝脂肪变性定义为HSI>30或FLI>60. 如果HSI和FLI中至少有一个有值, 则可用于评估; 如果两者都有值, 满足截断点足以诊断肝脂肪变性. 代谢失调需满足至少两种代谢风险异常: (1)白人男女腰围≥102/88 cm(或亚洲男女为≥90/80 cm); (2)血压≥130/85 mmHg; (3)甘油三酯升高(≥1.70 mmol/L); (4)高密度脂蛋白胆固醇降低(男<1.0 mmol/L, 女<1.3 mmol/L); (5)糖尿病前期(空腹血糖5.6-6.9 mmol/L, 餐后2 h血糖7.8-11.0 mmol/L, HbA1c: 5.7%-6.4%); (6)胰岛素抵抗评分≥2.5的稳态模型评估; 和(7)超敏C反应蛋白>2 mg/L[11]. 若受试者同时满足肝脏脂肪变性及上述任一代谢异常条件, 则赋值为1(患病); 若虽有脂肪变性但不满足代谢异常, 或无脂肪变性, 则赋值为0(非患病).
1.2.2 协变量及中介变量: 为了控制混杂因素对H. pylori与MAFLD关联的影响, 本研究纳入了多维度的协变量以提升结果可靠性. 社会人口学变量包括年龄(连续变量)、性别(1 = 男性, 2 = 女性)以及种族(分为墨西哥裔美国人、其他西班牙裔、非西班牙裔白人、非西班牙裔黑人及其他种族). 生活方式变量包括吸烟状态(定义为一生中吸烟是否达到100支)和饮酒状态(根据过去12 mo的饮酒频率判定), 身体测量指标包括体重指数(body mass index, BMI)和腰围. 此外, 合并症状态如2型糖尿病也被作为二分类协变量纳入分析模型, 因2型糖尿病与MAFLD互为因果, 会影响H. pylori相关的糖脂代谢紊乱程度[12]. 中介变量中所有生化指标均在NHANES实验室通过标准酶法、直接均相法或溴甲酚紫法等标准化程序测定, 确保了数据的跨样本可比性.
1.2.3 伦理知情同意: 本研究依托的美国NHANES数据库(https://www.cdc.gov/nchs/nhanes/), 已通过美国国家统计中心伦理审查委员会严格审批, 审查标准符合人体研究伦理规范. 所有参与者在纳入调查前, 均已充分知晓数据采集目的、生物样本使用范围及隐私保护措施, 自愿签署书面知情同意书(https://www.cdc.gov/nchs/nhanes/about/erb.html?CDC_AAref_Val=https://www.cdc.gov/nchs/nhanes/irba98.htm). 整个研究流程严格遵循《赫尔辛基宣言》中人体医学研究的伦理原则.
统计学处理 为比较研究样本的基线特征, 我们以平均±标准差连续变量评估连续变量, 分类变量用数字或百分比评估. 卡方检验(分类变量)和t检验(连续变量)用于评估基线差异. 调整协变量后, 使用多变量逻辑回归模型分析H. pylori感染和MAFLD风险之间的关联. 采用非参数bootstrap方法, 进行中介分析以评估血脂和肝功能指标在H. pylori感染和MAFLD之间的关联中的中介作用. 最后进行亚组分析以评估其他变量(性别、糖尿病、饮酒、吸烟、身体质量指数)对H. pylori感染和MAFLD风险之间关系的潜在调节作用. 所有统计分析均使用R软件(4.0版)和Python(3.8版)进行, P<0.05被认为具有统计学意义.
如表1所示, 根据纳入和排除标准, 本研究共纳入了4455名参与者. 参与者的平均年龄为46.07岁(标准差: 20.11岁), 女性占比为53.02%(2362人), 男性占比为46.98%(2093人), 女性人数略多于男性. 非感染组(n = 2525, 56.68%)和感染组(n = 1930, 43.32%). 与非感染组相比, 感染组参与者年龄更大(49.68岁 vs 43.31岁, P<0.001). 感染组中墨西哥裔美国人(42.85%)和非西班牙裔黑人(23.21%)的比例显著高于非感染组(分别为19.17%和14.85%), 而非感染组中非西班牙裔白人的比例更高(57.98% vs 22.49%, P<0.001). 在代谢相关指标方面, 感染组的BMI(28.35 kg/m2 vs 27.86 kg/m2, P = 0.010)和腰围(96.19 cm vs 95.10 cm, P = 0.019)均显著高于非感染组. 感染组的MAFLD患病率显著高于非感染组(74.25% vs 67.84%, P<0.001). 感染组的糖尿病患病率也显著高于非感染组(14.97% vs 8.24%, P<0.001). 在血脂指标方面, 感染组的总胆固醇(5.24 mmol/L vs 5.18 mmol/L, P = 0.060)和非高密度脂蛋白胆固醇(3.95 mmol/L vs 3.83 mmol/L, P<0.001)水平高于非感染组, 而高密度脂蛋白胆固醇水平低于非感染组(1.29 mmol/L vs 1.35 mmol/L, P<0.001). 在肝功能指标方面, 感染组的碱性磷酸酶(87.55 U/L vs 82.74 U/L, P<0.001)和γ-谷氨酰转移酶(34.18 U/L vs 29.59 U/L, P = 0.002)水平显著高于非感染组. 感染组的总蛋白水平高于非感染组(76.38 g/L vs 75.02 g/L, P<0.001), 而白蛋白水平低于非感染组(44.19 g/L vs 44.65 g/L, P<0.001). 感染组的饮酒率低于非感染组(74.77% vs 81.54%, P<0.001), 而吸烟率略高于非感染组(47.31% vs 43.64%, P = 0.015).
| 变量 | 总体(n = 4455) | 非H. pylori感染(n = 2525) | H. pylori感染(n = 1930) | P值 |
| 年龄(岁) | 46.07(20.11) | 43.31(20.04) | 49.68(19.63) | <0.001 |
| TC(mmol/L) | 5.21(1.09) | 5.18(1.09) | 5.24(1.10) | 0.060 |
| HDL-C(mmol/L) | 1.32(0.39) | 1.35(0.40) | 1.29(0.39) | <0.001 |
| non-HDL-C(mmol/L) | 3.88(1.09) | 3.83(1.07) | 3.95(1.10) | <0.001 |
| 总蛋白(g/L) | 75.61(4.87) | 75.02(4.82) | 76.38(4.81) | <0.001 |
| 白蛋白(g/L) | 44.45(3.55) | 44.65(3.70) | 44.19 (3.33) | <0.001 |
| ALT(U/L) | 26.19(30.23) | 25.44(30.90) | 27.16(29.32) | 0.058 |
| AST(U/L) | 24.92(21.74) | 24.49(24.05) | 25.49(18.28) | 0.114 |
| AST/ALT | 1.10(0.37) | 1.10(0.37) | 1.09(0.38) | 0.540 |
| 碱性磷酸酶(U/L) | 84.83(31.86) | 82.74(31.16) | 87.55(32.57) | <0.001 |
| GGT(U/L) | 31.58(50.12) | 29.59(50.32) | 34.18(49.75) | 0.002 |
| 总胆红素(μmol/L) | 9.71(5.03) | 9.77(5.34) | 9.62(4.58) | 0.321 |
| 糖化血红蛋白 | 5.50(1.09) | 5.36(0.91) | 5.69(1.27) | <0.001 |
| ISR | 1.18(1.12) | 0.30(0.19) | 2.33(0.74) | <0.001 |
| BMI | 28.08(6.25) | 27.86(6.29) | 28.35(6.20) | 0.010 |
| 腰围 | 95.57(15.45) | 95.10(15.80) | 96.19(14.97) | 0.019 |
| 性别 | ||||
| 男性 | 2093.00(46.98) | 1150.00(45.54) | 943.00(48.86) | 0.028 |
| 女性 | 2362.00(53.02) | 1375.00(54.46) | 987.00(51.14) | |
| 种族 | ||||
| 墨西哥裔美国人 | 1311.00(29.43) | 484.00(19.17) | 827.00(42.85) | <0.001 |
| 其他拉美裔 | 276.00(6.20) | 115.00(4.55) | 161.00(8.34) | |
| 非西班牙裔白人 | 1898.00(42.60) | 1464.00(57.98) | 434.00(22.49) | |
| 非西班牙裔黑人 | 823.00(18.47) | 375.00(14.85) | 448.00(23.21) | |
| 其他种族-包括多种族 | 147.00(3.30) | 87.00(3.45) | 60.00(3.11) | |
| MAFLD | ||||
| 否 | 1309.00(29.38) | 812.00(32.16) | 497.00(25.75) | <0.001 |
| 是 | 3146.00(70.62) | 1713.00(67.84) | 1433.00(74.25) | |
| 2型糖尿病 | ||||
| 否 | 3958.00(88.84) | 2317.00(91.76) | 1641.00(85.03) | <0.001 |
| 是 | 497.00(11.16) | 208.00(8.24) | 289.00(14.97) | |
| 是否饮酒 | ||||
| 否 | 953.00(21.39) | 466.00(18.46) | 487.00(25.23) | <0.001 |
| 是 | 3502.00(78.61) | 2059.00(81.54) | 1443.00(74.77) | |
| 是否吸烟 | ||||
| 否 | 2440.00(54.77) | 1423.00(56.36) | 1017.00(52.69) | 0.015 |
| 是 | 2015.00(45.23) | 1102.00(43.64) | 913.00(47.31) |
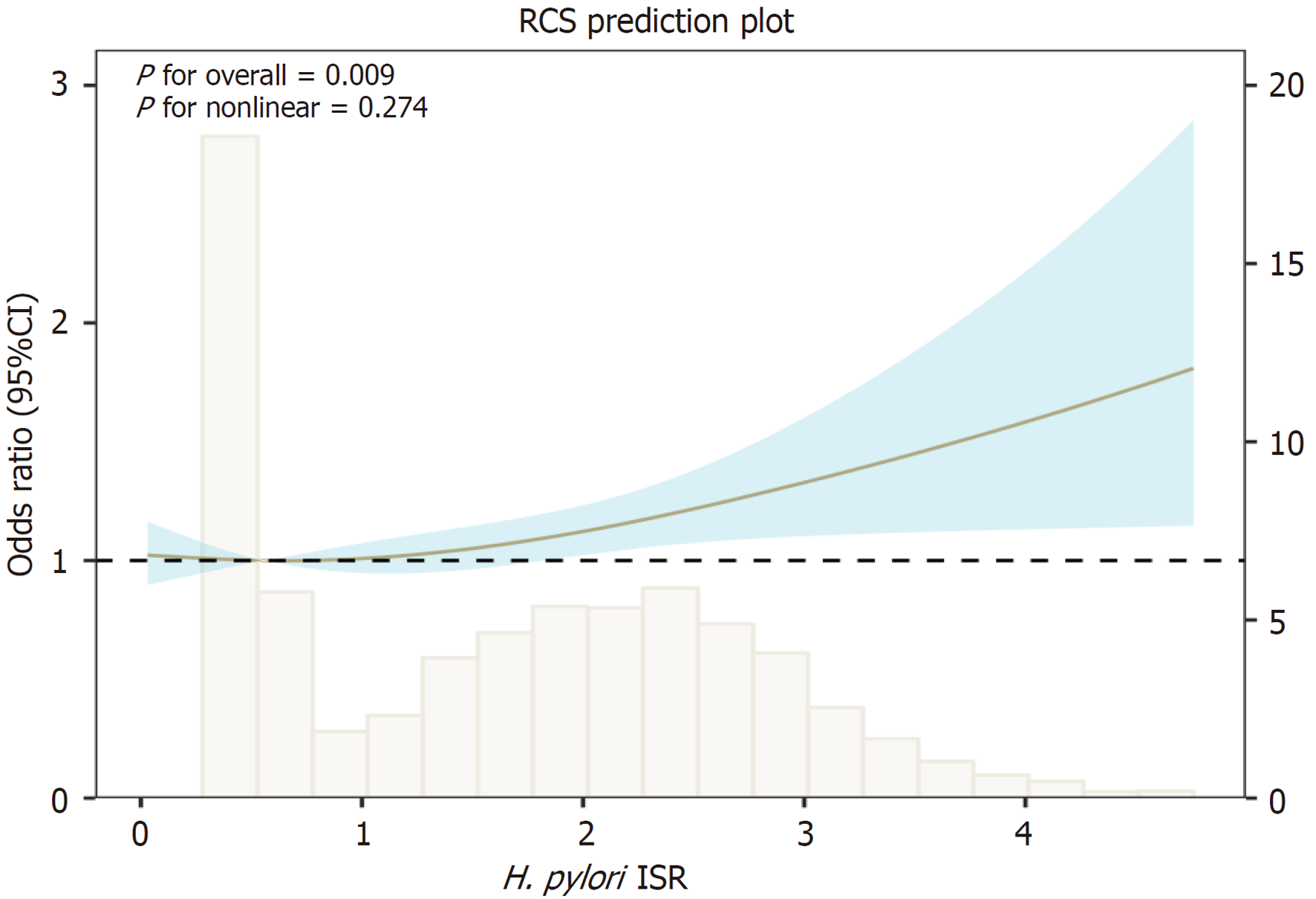
如表2所示, 在模型2中, 当H. pylori感染状态为分类变量时, 与未感染组相比, 感染组的MAFLD风险显著增加[比值比(odd ratio, OR) = 1.15(95%CI: 1.00-1.32); P = 0.045]. 当H. pylori ISR值为连续变量时, MAFLD的风险随着ISR值的增加而增加[OR = 1.10(95%CI: 1.03-1.17); P = 0.004]. 当ISR值被分组为三分位数时, 最高四分位数(Q3)组相对于最低四分位数(Q1)组MAFLD风险显著增加[OR = 1.24(95%CI: 1.05-1.47); P = 0.011], 而中间四分位数(Q2)组与最低四分位数(Q1)组相比, MAFLD风险无显著差异[OR = 1.04(95%CI: 0.88-1.22); P = 0.647]. 如图2所示, 进一步使用限制性三次样条模型研究H. pylori ISR值和MAFLD风险之间的剂量反应关系. ISR值和参与者的MAFLD风险之间存在非线性关系(P<0.05). 随着ISR值的增加, MAFLD的风险逐渐增加.
| 结局变量 | Crude model | Model 1 | Model 2 | |||||||||
| OR | Lower_OR | Upper_OR | P值 | OR | Lower_OR | Upper_OR | P值 | OR | Lower_OR | Upper_OR | P值 | |
| Non-H. pylori感染 | Reference | Reference | Reference | |||||||||
| H. pylori感染 | 1.3667 | 1.1983 | 1.5599 | 0.0000 | 1.2182 | 1.0641 | 1.3953 | 0.0043 | 1.1519 | 1.0034 | 1.3228 | 0.0449 |
| H. pylori_ISR | 1.1854 | 1.1169 | 1.2589 | 0.0000 | 1.1196 | 1.0532 | 1.1910 | 0.0003 | 1.0962 | 1.0303 | 1.1670 | 0.0038 |
| Q1 | Reference | Reference | Reference | |||||||||
| Q2 | 1.2016 | 1.0294 | 1.4032 | 0.0201 | 1.0973 | 0.9368 | 1.2855 | 0.2498 | 1.0382 | 0.8840 | 1.2195 | 0.6474 |
| Q3 | 1.5330 | 1.3082 | 1.7978 | 0.0000 | 1.3256 | 1.1259 | 1.5615 | 0.0007 | 1.2421 | 1.0521 | 1.4671 | 0.0106 |
2.3.1 脂质分布的中介作用: 如表3所示, 当H. pylori感染状态(分类变量)作为暴露变量时, 脂质参数的中介分析显示: TC的中介作用不显著[间接效应(average causal mediation effects, ACME) = 0.0045(95%CI: -0.00002至0.0095); P = 0.054], 中介比例为7.07%(P = 0.054). 低密度脂蛋白胆固醇(non-high-density lipoprotein, non-HDL)的中介作用显著[ACME = 0.014(95%CI: 0.0066-0.0217); P<0.001], 其中介比例为22.03%(95%CI: 10.98%-38.62%; P<0.001). 高密度脂蛋白胆固醇(high-density lipoprotein, HDL)的中介作用显著[ACME = 0.0196(95%CI: 0.0124-0.0271); P<0.001], 其中介比例为30.61%(95%CI: 18.55%-50.09%; P<0.001).
| Estimate | CI_Lower95 | CI_Upper95 | P值 | |
| TC | ||||
| ACME | 0.0045 | 0.0000 | 0.0095 | 0.0540 |
| ADE | 0.0595 | 0.0345 | 0.0852 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.0707 | -0.0004 | 0.1615 | 0.0540 |
| non LDL | ||||
| ACME | 0.0141 | 0.0066 | 0.0217 | 0.0000 |
| ADE | 0.0500 | 0.0248 | 0.0756 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.2203 | 0.1098 | 0.3862 | 0.0000 |
| HDL | ||||
| ACME | 0.0196 | 0.0124 | 0.0271 | 0.0000 |
| ADE | 0.0445 | 0.0201 | 0.0695 | 0.0040 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.3061 | 0.1855 | 0.5009 | 0.0000 |
当使用H. pylori ISR值(连续变量)作为暴露变量时, 脂质参数的中介分析显示(表4), TC具有显著的中介效应[ACME = 0.0025(95%CI: 0.0005-0.0047); P = 0.014], 中介比例为7.48%(95%CI: 1.80%-14.33%; P = 0.014). 非高密度脂蛋白胆固醇具有显著的中介作用[ACME = 0.0078(95%CI: 0.0046-0.0110); P<0.001], 中介比例为22.99%(95%CI: 13.38%-36.15%; P<0.001). 高密度脂蛋白胆固醇的中介作用显著[ACME = 0.0106(95%CI: 0.0073-0.0140); P<0.001], 其中介比例达31.09%(95%CI: 21.23%-45.55%; P<0.001).
| Estimate | CI_Lower95 | CI_Upper95 | P值 | |
| TC | ||||
| ACME | 0.0025 | 0.0005 | 0.0047 | 0.0140 |
| ADE | 0.0314 | 0.0200 | 0.0433 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.0748 | 0.0180 | 0.1433 | 0.0140 |
| non HDL | ||||
| ACME | 0.0078 | 0.0046 | 0.0110 | 0.0000 |
| ADE | 0.0261 | 0.0153 | 0.0376 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.2299 | 0.1338 | 0.3615 | 0.0000 |
| HDL | ||||
| ACME | 0.0105 | 0.0073 | 0.0140 | 0.0000 |
| ADE | 0.0234 | 0.0126 | 0.0342 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.3109 | 0.2123 | 0.4555 | 0.0000 |
2.3.2 肝功能的中介作用: 如表5所示, 当幽门螺旋杆菌感染状态(分类变量)用作暴露变量时, 肝功能指标的中介分析显示: 丙氨酸氨基转移酶(alanine aminotransferase, ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase, AST)、AST/ALT比值以及胆红素的中介效应均不显著(P>0.05). γ-谷氨酰转移酶(γ-glutamyl transferase, GGT)的中介效应显著[ACME = 0.0022(95%CI: 0.0005-0.0050); P = 0.004], 中介百分比为3.48%(95%CI: 0.86%-9.08%; P = 0.004). 碱性磷酸酶的介导作用是显著的[ACME = 0.0052(95%CI: 0.0026-0.0088); P<0.001], 中介百分比为8.18%(95%CI: 3.93%-16.08%; P<0.001). 白蛋白具有显著的中介作用[ACME = 0.0120(95%CI: 0.0068-0.0178); P<0.001], 中介百分比为18.77%(95%CI: 10.05%-34.62%; P<0.001). 总蛋白具有显著的中介效应[ACME = -0.0115(95%CI: -0.0160至-0.0073); P<0.001], 中介百分比为-17.93%(95%CI: -32.48%至-10.14%; P<0.001).
| Estimate | CI_Lower95 | CI_Upper95 | P值 | |
| ALT | ||||
| ACME | 0.0018 | -0.0001 | 0.0067 | 0.0760 |
| ADE | 0.0622 | 0.0355 | 0.0887 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.0286 | -0.0010 | 0.1160 | 0.0760 |
| AST | ||||
| ACME | -0.0002 | -0.0009 | 0.0012 | 0.7680 |
| ADE | 0.0643 | 0.0384 | 0.0904 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | -0.0029 | -0.0144 | 0.0220 | 0.7680 |
| AST/ALT | ||||
| ACME | 0.0025 | -0.0050 | 0.0104 | 0.5360 |
| ADE | 0.0616 | 0.0381 | 0.0869 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.0386 | -0.1026 | 0.1537 | 0.5360 |
| GGT | ||||
| ACME | 0.0022 | 0.0005 | 0.0050 | 0.0040 |
| ADE | 0.0618 | 0.0355 | 0.0880 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.0348 | 0.0086 | 0.0908 | 0.0040 |
| Alkaline phosphotase (U/L) | ||||
| ACME | 0.0052 | 0.0026 | 0.0088 | 0.0000 |
| ADE | 0.0588 | 0.0328 | 0.0852 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.0818 | 0.0393 | 0.1608 | 0.0000 |
| Bilirubin, total (μmol/L) | ||||
| ACME | 0.0016 | -0.0016 | 0.0051 | 0.3240 |
| ADE | 0.0625 | 0.0364 | 0.0894 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.0251 | -0.0266 | 0.0852 | 0.3240 |
| Albumin (g/L) | ||||
| ACME | 0.0120 | 0.0068 | 0.0178 | 0.0000 |
| ADE | 0.0520 | 0.0263 | 0.0775 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | 0.1877 | 0.1005 | 0.3462 | 0.0000 |
| Protein, total (g/L) | ||||
| ACME | -0.0115 | -0.0160 | -0.0073 | 0.0000 |
| ADE | 0.0756 | 0.0498 | 0.1027 | 0.0000 |
| Total effect | 0.0641 | 0.0383 | 0.0902 | 0.0000 |
| Prop mediated | -0.1793 | -0.3248 | -0.1014 | 0.0000 |
如表6所示, 当幽门螺旋杆菌ISR值(连续变量)作为暴露变量时, 肝功能指标的中介分析显示: AST、ALT、AST/ALT比值及总胆红素的中介作用不显著(P>0.05). GGT的中介作用是显著的[ACME = 0.0007(95%CI: 0.0001-0.0017); P = 0.006], 中介百分比为2.02%(95%CI: 0.43%-5.35%; P = 0.006). 碱性磷酸酶的中介作用同样显著[ACME = 0.0015(95%CI: 0.0006-0.0028); P<0.001], 中介百分比为4.47%(95%CI: 1.85%-8.92%; P<0.001). 白蛋白也具有显著的中介作用[ACME = 0.0039(95%CI: 0.0016-0.0063); P<0.001], 中介百分比为11.39%(95%CI: 4.75%-21.22%; P<0.001). 总蛋白具有显著的中介效应[ACME = -0.0052(95%CI: -0.0071至-0.0034); P<0.001], 中介百分比为-15.33%(95%CI: -25.84%至-9.33%; P<0.001).
| Estimate | CI_Lower95 | CI_Upper95 | P值 | |
| ALT | ||||
| ACME | 0.0005 | -0.0001 | 0.0021 | 0.1340 |
| ADE | 0.0334 | 0.0219 | 0.0452 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.0143 | -0.0031 | 0.0649 | 0.1340 |
| AST | ||||
| ACME | -0.0001 | -0.0003 | 0.0004 | 0.8640 |
| ADE | 0.0340 | 0.0224 | 0.0458 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | -0.0015 | -0.0081 | 0.0119 | 0.8640 |
| AST/ALT | ||||
| ACME | 0.0011 | -0.0022 | 0.0047 | 0.5260 |
| ADE | 0.0328 | 0.0220 | 0.0438 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.0333 | -0.0772 | 0.1312 | 0.5260 |
| GGT | ||||
| ACME | 0.0007 | 0.0001 | 0.0017 | 0.0060 |
| ADE | 0.0332 | 0.0220 | 0.0449 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.0202 | 0.0043 | 0.0535 | 0.0060 |
| Alkaline phosphotase (U/L) | ||||
| ACME | 0.0015 | 0.0006 | 0.0028 | 0.0000 |
| ADE | 0.0324 | 0.0209 | 0.0445 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.0447 | 0.0185 | 0.0892 | 0.0000 |
| Bilirubin, total (μmol/L) | ||||
| ACME | -0.0005 | -0.0019 | 0.0009 | 0.4760 |
| ADE | 0.0345 | 0.0232 | 0.0463 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | -0.0161 | -0.0658 | 0.0263 | 0.4760 |
| Albumin (g/L) | ||||
| ACME | 0.0039 | 0.0016 | 0.0063 | 0.0000 |
| ADE | 0.0301 | 0.0188 | 0.0414 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | 0.1139 | 0.0475 | 0.2122 | 0.0000 |
| Protein, total (g/L) | ||||
| ACME | -0.0052 | -0.0071 | -0.0034 | 0.0000 |
| ADE | 0.0391 | 0.0276 | 0.0513 | 0.0000 |
| Total effect | 0.0339 | 0.0225 | 0.0458 | 0.0000 |
| Prop mediated | -0.1533 | -0.2584 | -0.0933 | 0.0000 |
上述结果表明, 血脂指标(特别是非高密度脂蛋白胆固醇和高密度脂蛋白胆固醇)和部分肝功能指标(如碱性磷酸酶、白蛋白、GGT)在H. pylori感染与MAFLD的关联中发挥了显著的中介作用.
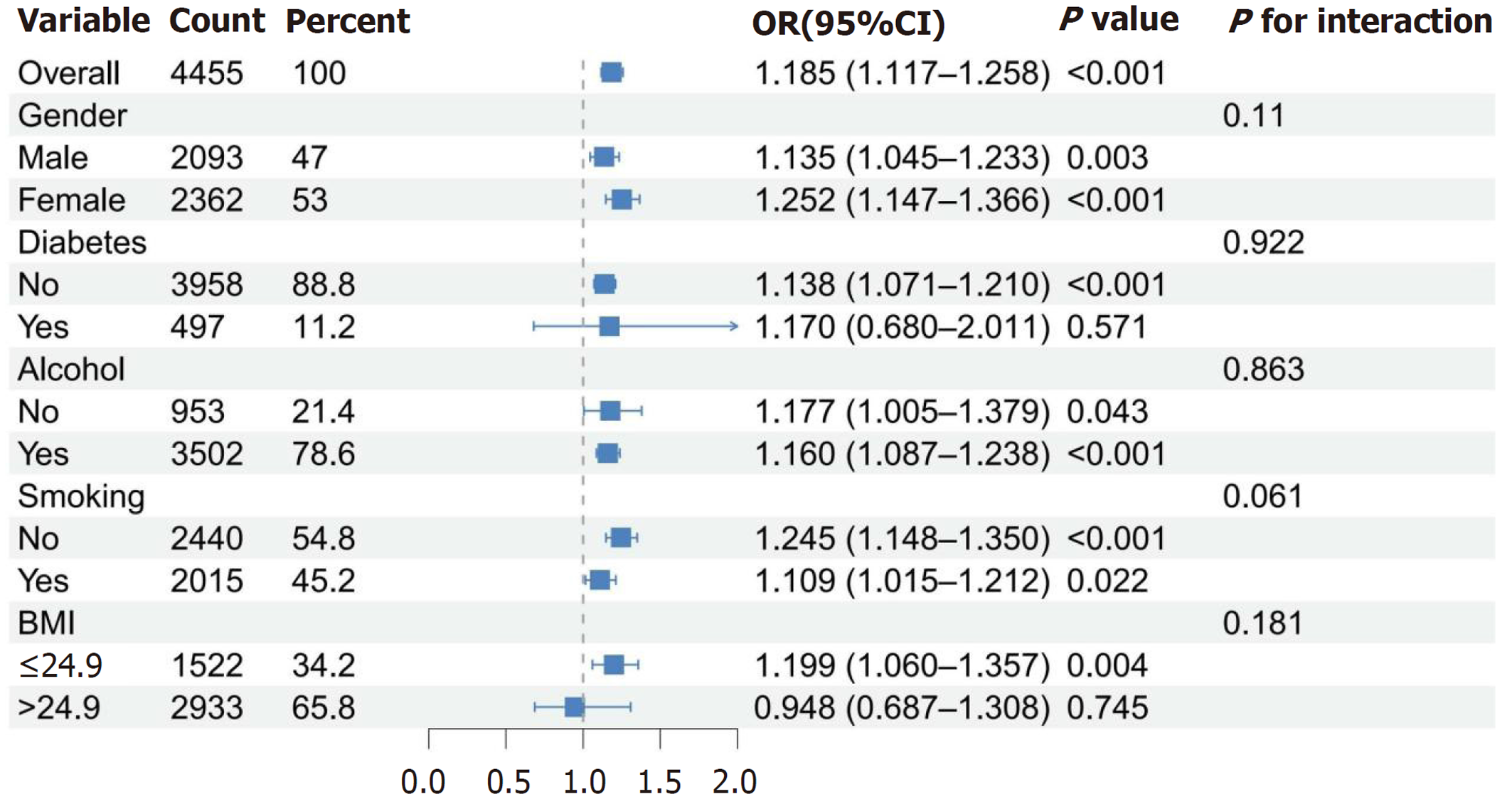
如图3所示, 交互作用检验显示, 各亚组间H. pylori ISR值与MAFLD风险的关联均无统计学显著差异(所有交互作用P>0.05), 表明性别、BMI、吸烟、饮酒、糖尿病因素均未显著影响H. pylori ISR值与MAFLD风险之间的关联. 在总人群中, H. pylori ISR值与MAFLD风险显著相关[OR = 1.185(95%CI: 1.117-1.258); P<0.001]. 在性别亚组中, 男性[OR = 1.135(95%CI: 1.045-1.233); P = 0.003]和女性[OR = 1.252(95%CI: 1.147-1.366); P<0.001]均显示H. pylori ISR值与MAFLD风险存在显著正相关, 交互作用P值为0.11. 在糖尿病亚组中, 非糖尿病患者[OR = 1.138(95%CI: 1.071-1.210); P<0.001]显示显著关联, 而糖尿病患者[OR = 1.170(95%CI: 0.680至2.011); P = 0.571]未显示显著关联, 交互作用P值为0.922. 在饮酒亚组中, 不饮酒者[OR = 1.177(95%CI: 1.005-1.379); P = 0.043]和饮酒者[OR = 1.160(95%CI: 1.087-1.238); P<0.001]均显示显著关联, 交互作用P值为0.863. 在吸烟亚组中, 不吸烟者[OR = 1.245(95%CI: 1.148-1.350); P<0.001]和吸烟者[OR = 1.109(95%CI: 1.015-1.212); P = 0.022]均显示显著关联, 交互作用P值为0.061. 在BMI亚组中, BMI≤24.9 kg/m²组[OR = 1.199(95%CI: 1.060-1.357); P = 0.004]显示显著关联, 而BMI>24.9 kg/m²组[OR = 0.948(95%CI: 0.687-1.308); P = 0.745]未显示显著关联, 交互作用P值为0.181. 上述结果表明年龄、糖尿病、吸烟、饮酒、BMI均不是ISR对MAFLD影响的效应修饰因素, 但值得注意的是在吸烟亚组中交互作用P值为0.061(接近0.05阈值), 尚不能明确吸烟并非的效应修饰因素, 需更大样本进行验证.
研究通过多变量逻辑回归模型渐进调整年龄、性别、吸烟、饮酒及糖尿病等多种潜在混杂因素后, 结果显示H. pylori仍与MAFLD风险显著相关, 提示H. pylori可能是MAFLD的独立危险因素. 以分类变量(感染/非感染)分析时, 感染组MAFLD患病风险较非感染组显著升高(OR = 1.15, 95%CI: 1.00-1.32, P = 0.045); 以感染强度指标(H. pylori ISR值)作为连续变量时, 其每升高1个单位, MAFLD风险显著增加(OR = 1.10, 95%CI: 1.03-1.17, P = 0.004), 两种暴露形式的一致性结果, 表明该关联具有较好的稳健性. 如限制性立方样条模型所示, H. pylori感染强度与MAFLD风险之间并非简单的线性关系, 而是存在一定的剂量反应特征. 该发现具有重要的流行病学意义, 提示H. pylori对MAFLD的影响可能与感染负荷或者持续时间相关, 而不仅仅取决于是否感染来判定.
研究结果显示, 血脂代谢指标, 尤其是non-HDL升高和HDL降低, 构成了H. pylori影响MAFLD风险的最主要中介路径. 在分类变量及连续变量中, non-HDL和HDL均表现出显著的中介效应, 两者合计解释了超过50%的总效应, 提示血脂代谢紊乱在H. pylori与MAFLD关联中处于核心地位.
值得注意的是, HDL降低在该关联中的中介效应更为突出, 其中介比例甚至高于non-HDL. 既往研究表明[13,14], H. pylori感染可通过诱导慢性低度炎症状态, 导致HDL-C水平下降, 且在成功根除感染后HDL水平可部分恢复, 提示H. pylori对HDL具有潜在的可逆性影响. HDL传统上被视为"保护性脂蛋白", 但近年来研究[15,16]逐渐认识到, HDL在代谢性疾病中的作用不仅体现在数量下降, 更重要的是其功能受损. 本研究中HDL显著的中介效应提示, H. pylori可能通过影响HDL水平及其相关功能, 削弱机体清除肝脏和外周组织中过量脂质的能力, 从而为肝内脂肪积聚创造有利条件.
本研究的中介分析结果显示, 无论分类变量、连续变量, non-HDL在H. pylori与MAFLD关联中占据约22%的中介比例, 两种暴露形式下结果高度一致, 提示该通路具有较高的稳定性. 既往研究表明[17], H. pylori可显著升高多种促炎细胞因子水平, 包括肿瘤坏死因子α(tumor necrosis factor alpha, TNF-α)和白介素-6(interleukin-6, IL-6)等, 这些炎症因子在脂代谢调控中具有关键作用. 例如, TNF-α通过抑制脂蛋白脂肪酶活性, 减少外周组织对极低密度脂蛋白的清除, 从而导致富含甘油三酯和胆固醇的脂蛋白在循环中蓄积[18,19]. IL-6则通过激活JAK-STAT及NF-κB等信号通路, 干扰肝脏脂质合成、分泌及清除过程, 进一步加剧脂蛋白代谢紊乱[20]. 并且本次研究中的亚组分析也显示, H. pylori感染和MAFLD之间的联系在低体重指数人群中特别显著, 这可能与该组中炎症因子的相对高表达有关. 本研究从大规模人群层面量化了这一潜在路径的中介效应, 为炎症驱动的脂代谢异常在H. pylori相关MAFLD中的作用提供了新的流行病学证据, 也为低BMI等特定人群的风险干预提供了靶点参考.
肠道微生物群介导的胆汁酸代谢异常(abnormal bile acid metabolism, ABAM)与HDL显著降低高度相关(中介比例30.61%). HDL水平受法尼类X受体信号通路的调节, 其降低与肠道微生物群生态失调引起的继发性胆汁酸积累机制有关[21,22]. 本研究中HDL显著的中介效应, 提示H. pylori可能通过肠道菌群介导的胆汁酸代谢异常, 抑制HDL的合成或功能. 具体来说, H. pylori可升高胃泌素水平, 破坏回肠FXR-FGF19轴的正常负反馈调节, 导致胆汁酸池扩大及次级胆汁酸积累, 进而抑制HDL成熟并削弱逆向胆固醇转运能力[23-25]. 同时, 高密度脂蛋白降低发生在H. pylori感染小鼠模型中, 补充法尼类X受体激动剂可以部分逆转这种变化, 进一步为这一假说提供了证据[26]. 此外, 研究中HDL减少和碱性磷酸酶(alkaline phosphatase, ALP)增加的协同出现可能反映了胆汁淤积下肝细胞的应激反应, 即胆汁酸蓄积可通过激活c-Jun氨基末端激酶等应激通路, 诱导碱性磷酸酶分泌增加, 从而进一步加重肝脏代谢负担[27].
值得注意的是ALP和白蛋白在本研究中也表现出显著的中介作用, 尽管这些指标的整体比例低于non-HDL和HDL, 但其指标统计学显著性及方向的一致性提示, 它们可能反映了肝脏层面多条病理生理通路的综合效应, 而非单一单纯的肝细胞损伤进程. 升高的ALP可能不仅反映了ABAM诱导的肝细胞或胆管上皮细胞的应激[28]. 白蛋白水平降低, 除了表明肝脏合成功能受损外, 还可能与血管通透性增加、白蛋白外渗和全身炎症条件下的营养代谢功能障碍等多种因素有关[29]. 这两个指标可以与前面提到的炎症因子和ABAM的激活形成相互加剧的恶性循环. 例如, 促炎细胞因子如IL-6可以通过激活JAK-STAT信号通路诱导肝细胞凋亡并抑制白蛋白mRNA的转录和合成[30]. 次级胆汁酸, 尤其是脱氧胆酸的积累可通过诱导线粒体功能障碍、内质网应激、细胞膜流动性改变等进一步加重肝细胞损伤和功能障碍[31]. 反之, 肝细胞损伤促进更多炎症介质的释放, 削弱胆汁酸解毒和排泄的能力[32]. 此次研究观察到不同介质的协同变化, 与基础实验模型中观察到的多途径相互作用一致, 如NF-κB和FXR信号通路之间的交叉抑制[33,34], 以及肠道微生物群生态失调和肝脏炎症之间的肠道-肝脏轴对话[35]. 总之, 这些表明H. pylori感染可能通过多种平行和交织的途径形成, 包括持续低度炎症、胆汁酸代谢障碍和直接或间接的肝毒性作用, 这些因素共同促进了MAFLD的发生和发展.
本研究具有一定的临床意义. 对于患有并发H. pylori感染的MAFLD患者, 尤其是非肥胖个体, H. pylori感染根除治疗可能提供除改善胃肠道症状之外的额外代谢益处. 通过清除感染, 它可能有助于减少慢性低度炎症, 调节肠道微生物群和胆汁酸代谢, 从而改善致动脉粥样硬化, 脂质谱和一些肝功能指标, 并最终潜在地延缓MAFLD的进展. 非高密度脂蛋白和高密度脂蛋白等指标可以作为潜在的生物标志物, 用于评估H. pylori感染相关的MAFLD风险和干预的有效性.
这项研究揭示了H. pylori感染和MAFLD风险之间的显著相关性, 并首次量化了脂代谢标志物的关键介导作用. 这些发现不仅加深了我们对MAFLD多因素发病机制的理解, 强调了在代谢性肝病的管理中关注慢性感染因素的重要性, 而且为未来针对性的病因干预和风险分层提供了坚实的科学基础和新的研究视角.
在代谢功能障碍相关脂肪性肝病(metabolic dysfunction-associated fatty liver disease, MAFLD)复杂的多病因发病网络中, 除了经典的代谢危险因素, 慢性感染与炎症状态的作用日益受到关注. 揭示慢性炎症与MAFLD的相关性及代谢指标在其中的中介作用机制, 能够为MASLD的防治及危险分层提供新的思路以及理论基础.
幽门螺旋杆菌(Helicobacter pylori, H. pylori)感染与多种代谢异常存在潜在关联. 因此, H. pylori感染可能通过炎症与代谢交互通路参与MAFLD的发生发展过程, 本研究首次量化证实, 血脂代谢指标及肝功能指标在两者之间的联系, 为未来开展针对性的病因干预、降低人群疾病负担提供了坚实的科学依据.
本研究旨在探讨H. pylori感染与MAFLD风险之间的关联, 并定量评估血脂代谢指标与肝功能指标在两者关系中的中介作用, 以揭示H. pylori感染影响MAFLD的潜在代谢路径. 本研究是首次研究了代谢指标及炎症作用在两个疾病之间的中介作用, 为MAFLD风险因素提供证据. 同时首次H. pylori ISR值与MAFLD发病风险程度的关系, 便于对疾病进行风险评估, 实现早期干预及预防.
本研究数据来自于美国国家健康和营养调查数据库, 该数据库具有随机性、样本量大、指标齐全等优点. 本研究回顾性的分析了H. pylori感染与MAFLD的相关性, 首先, 通过纳入和排除标准选取一定数量的参与者, 所分析数据包含了年龄、种族、实验室指标、生活状态、身体测量指标, 尽可能纳入了多方面的潜在因素, 以提高研究的可靠性. 其次, 通过多变量逻辑回归模型控制混杂因素, 探索了H. pylori感染与MAFLD的独立相关性. 同时, 通过限制性立方样条分析探索了H. pylori ISR值与MAFLD疾病发病风险的关系. 为定量评估血脂及肝功能指标在H. pylori感染影响MAFLD过程中的贡献, 本研究采用非参数Bootstrap中介分析方法, 通过1000次重复抽样构建抽样分布, 精准估算直接效应、间接效应及中介比例. 该方法无需假设数据正态分布, 对小样本或非正态数据的效应估计更稳健. 最后, 为探究关联强度的人群异质性, 研究进一步对关键协变量进行分层亚组分析, 通过交互作用检验评估不同特征人群中关联强度的异质性.
本研究发现: (1)通过多变量逻辑回归模型调整多种潜在混杂因素后, 结果显示H. pylori感染仍与MAFLD风险显著相关, 提示其可能是MAFLD的独立危险因素; (2)H. pylori感染强度(ISR值)与MAFLD风险之间并非简单的线性关系, 而是存在一定的剂量反应特征; (3)无论以H. pylori感染作为分类变量和连续变量, 非高密度脂蛋白胆固醇和高密度脂蛋白胆固醇均表现出显著的中介效应, 两者合计解释了超过50%的总效应; 和(4)碱性磷酸酶、白蛋白以及γ-谷氨酰转移酶等多项和肝功能相关指标在H. pylori感染与MAFLD之间发挥了显著的中介作用.
H. pylori感染与MAFLD风险的显著正相关, 且该关联存在剂量-反应特征, 随着ISR值升高, MAFLD患病风险逐渐增加. 并且研究首次量化证实, 血脂代谢紊乱是两者关联的核心中介路径.
未来需要进行大规模的前瞻性队列研究, 以明确H. pylori感染早于MAFLD发生的时间顺序, 并长期随访量化感染负荷对MAFLD发病及进展的长期风险. 机制研究需要更加深入, 例如使用动物模型或细胞实验来探索特定H. pylori感染毒力因子是否通过上述炎症、微生物群或激素途径直接或间接发挥作用. 此外, 通过多组学技术量化每个途径的相对贡献, 并探索H. pylori感染、宿主遗传背景、肠道微生物群和饮食因素之间的复杂相互作用, 将有助于识别高危人群, 并最终为制定个性化预防和管理策略提供精确的基础.
| 1. | Dong W, Zhang H, Mu S, Shi S, Zhang J, Xu K. Advances in Incretin-Based Therapies for MAFLD: Mechanisms and Clinical Evidence. Clin Pharmacol Ther. 2026;119:336-349. [PubMed] [DOI] |
| 2. | Hu Z, Yue H, Jiang N, Qiao L. Diet, oxidative stress and MAFLD: a mini review. Front Nutr. 2025;12:1539578. [PubMed] [DOI] |
| 3. | Lenart-Lipińska M, Łuniewski M, Szydełko J, Matyjaszek-Matuszek B. Clinical and Therapeutic Implications of Male Obesity. J Clin Med. 2023;12:5354. [PubMed] [DOI] |
| 4. | Liu Q, Shang Y, Shen L, Yu X, Cao Y, Zeng L, Zhang H, Rao Z, Li Y, Tao Z, Liu Z, Huang X. Outer membrane vesicles from genetically engineered Salmonella enterica serovar Typhimurium presenting Helicobacter pylori antigens UreB and CagA induce protection against Helicobacter pylori infection in mice. Virulence. 2024;15:2367783. [PubMed] [DOI] |
| 5. | Kountouras J, Polyzos SA, Doulberis M, Zeglinas C, Artemaki F, Vardaka E, Deretzi G, Giartza-Taxidou E, Tzivras D, Vlachaki E, Kazakos E, Katsinelos P, Mantzoros CS. Potential impact of Helicobacter pylori-related metabolic syndrome on upper and lower gastrointestinal tract oncogenesis. Metabolism. 2018;87:18-24. [PubMed] [DOI] |
| 8. | Zhang J, Hai X, Wang S, Zhu F, Gu Y, Meng G, Zhang Q, Liu L, Wu H, Zhang S, Zhang T, Wang X, Sun S, Zhou M, Jia Q, Song K, Niu K. Helicobacter pylori infection increase the risk of subclinical hyperthyroidism in middle-aged and elderly women independent of dietary factors: Results from the Tianjin chronic low-grade systemic inflammation and health cohort study in China. Front Nutr. 2023;10:1002359. [PubMed] [DOI] |
| 9. | Tang L, Xie P, Wang H, Hong X, Gong Z, Zhao G, Yue M. The sex hormone-gut microbiome axis: mechanistic drivers of sex-disparate bacterial infection outcomes and precision clinical interventions. Clin Microbiol Rev. 2025;38:e0023625. [PubMed] [DOI] |
| 10. | Xiong C, Chen Z, Wu X, Zhang C, Yuan Z, Wang X, Xiao Z, Chen Y, Deng S, Wu X, Li M, Du F, Zhao Y, Li X, He X, Shen J. The impact of multidimensional interactions among Helicobacter pylori infection, tumor microenvironment, and gut microbiota on gastric cancer immune response. Eur J Pharmacol. 2026;1011:178401. [PubMed] [DOI] |
| 11. | Eslam M, Newsome PN, Sarin SK, Anstee QM, Targher G, Romero-Gomez M, Zelber-Sagi S, Wai-Sun Wong V, Dufour JF, Schattenberg JM, Kawaguchi T, Arrese M, Valenti L, Shiha G, Tiribelli C, Yki-Järvinen H, Fan JG, Grønbæk H, Yilmaz Y, Cortez-Pinto H, Oliveira CP, Bedossa P, Adams LA, Zheng MH, Fouad Y, Chan WK, Mendez-Sanchez N, Ahn SH, Castera L, Bugianesi E, Ratziu V, George J. A new definition for metabolic dysfunction-associated fatty liver disease: An international expert consensus statement. J Hepatol. 2020;73:202-209. [PubMed] [DOI] |
| 12. | Gao S, Zhang Y, Liang K, Bi R, Du Y. Mesenchymal Stem Cells (MSCs): A Novel Therapy for Type 2 Diabetes. Stem Cells Int. 2022;2022:8637493. [PubMed] [DOI] |
| 13. | Scharnagl H, Kist M, Grawitz AB, Koenig W, Wieland H, März W. Effect of Helicobacter pylori eradication on high-density lipoprotein cholesterol. Am J Cardiol. 2004;93:219-220. [PubMed] [DOI] |
| 14. | 余 晗俏, 李 超, 余 育斌, 冯 丽娜, 盛 晓生, 王 林燕, 叶 晓霞. Hp感染根除疗法对慢性冠脉综合征Gensini积分和脂代谢及预后的影响. 中华医院感染学杂志. 2022;32:2131-2136. [DOI] |
| 15. | Chiesa ST, Charakida M. High-Density Lipoprotein Function and Dysfunction in Health and Disease. Cardiovasc Drugs Ther. 2019;33:207-219. [PubMed] [DOI] |
| 16. | Madaudo C, Bono G, Ortello A, Astuti G, Mingoia G, Galassi AR, Sucato V. Dysfunctional High-Density Lipoprotein Cholesterol and Coronary Artery Disease: A Narrative Review. J Pers Med. 2024;14:996. [PubMed] [DOI] |
| 17. | Krauss RM, Grunfeld C, Doerrler WT, Feingold KR. Tumor necrosis factor acutely increases plasma levels of very low density lipoproteins of normal size and composition. Endocrinology. 1990;127:1016-1021. [PubMed] [DOI] |
| 18. | Zhao XX, Liu MH, Wang RL, Tian T. Effect of Gender and Age on the Correlation between Helicobacter pylori and Colorectal Adenomatous Polyps in a Chinese Urban Population: A Single Center Study. Gastroenterol Res Pract. 2020;2020:8596038. [PubMed] [DOI] |
| 19. | Yu B, de Vos D, Guo X, Peng S, Xie W, Peppelenbosch MP, Fu Y, Fuhler GM. IL-6 facilitates cross-talk between epithelial cells and tumor- associated macrophages in Helicobacter pylori-linked gastric carcinogenesis. Neoplasia. 2024;50:100981. [PubMed] [DOI] |
| 20. | Sparks JD, Cianci J, Jokinen J, Chen LS, Sparks CE. Interleukin-6 mediates hepatic hypersecretion of apolipoprotein B. Am J Physiol Gastrointest Liver Physiol. 2010;299:G980-G989. [PubMed] [DOI] |
| 21. | Dong B, Young M, Liu X, Singh AB, Liu J. Regulation of lipid metabolism by obeticholic acid in hyperlipidemic hamsters. J Lipid Res. 2017;58:350-363. [PubMed] [DOI] |
| 22. | Gautier T, de Haan W, Grober J, Ye D, Bahr MJ, Claudel T, Nijstad N, Van Berkel TJC, Havekes LM, Manns MP, Willems SM, Hogendoorn PCW, Lagrost L, Kuipers F, Van Eck M, Rensen PCN, Tietge UJF. Farnesoid X receptor activation increases cholesteryl ester transfer protein expression in humans and transgenic mice. J Lipid Res. 2013;54:2195-2205. [PubMed] [DOI] |
| 23. | Thain A, Hart K, Ahmadi KR. Addressing the Gaps in the Vitamin B12 Deficiency 2024 NICE Guidelines: Highlighting the Need for Better Recognition, Diagnosis, and Management of Pernicious Anaemia. Eur J Clin Nutr. 2025;79:607-610. [PubMed] [DOI] |
| 24. | Gunawardhana N, Jang S, Choi YH, Hong YA, Jeon YE, Kim A, Su H, Kim JH, Yoo YJ, Merrell DS, Kim J, Cha JH. Helicobacter pylori-Induced HB-EGF Upregulates Gastrin Expression via the EGF Receptor, C-Raf, Mek1, and Erk2 in the MAPK Pathway. Front Cell Infect Microbiol. 2017;7:541. [PubMed] [DOI] |
| 25. | Liao Y, Wang L, Liu F, Zhou Y, Lin X, Zhao Z, Xu S, Tang D, Jiao Y, Yang L, Yu W, Gao P. Emerging trends and hotspots in metabolic dysfunction-associated fatty liver disease (MAFLD) research from 2012 to 2021: A bibliometric analysis. Front Endocrinol (Lausanne). 2023;14:1078149. [PubMed] [DOI] |
| 26. | Tomasini S, Vigo P, Margiotta F, Scheele US, Panella R, Kauppinen S. The Role of microRNA-22 in Metabolism. Int J Mol Sci. 2025;26:782. [PubMed] [DOI] |
| 27. | Chapman MJ. HDL functionality in type 1 and type 2 diabetes: new insights. Curr Opin Endocrinol Diabetes Obes. 2022;29:112-123. [PubMed] [DOI] |
| 28. | Xu Q, Zhu W, Yin Y. Diagnostic value of anti-mitochondrial antibody in patients with primary biliary cholangitis: A systemic review and meta-analysis. Medicine (Baltimore). 2023;102:e36039. [PubMed] [DOI] |
| 29. | Xie Y, He C, Wang W. Prognostic nutritional index: A potential biomarker for predicting the prognosis of decompensated liver cirrhosis. Front Nutr. 2022;9:1092059. [PubMed] [DOI] |
| 30. | Calvez V, Becherucci G, Covello C, Piccirilli G, Mignini I, Esposto G, Laterza L, Ainora ME, Scaldaferri F, Gasbarrini A, Zocco MA. Navigating the Intersection: Sarcopenia and Sarcopenic Obesity in Inflammatory Bowel Disease. Biomedicines. 2024;12:1218. [PubMed] [DOI] |
| 31. | Ren Z, Zhao L, Zhao M, Bao T, Chen T, Zhao A, Zheng X, Gu X, Sun T, Guo Y, Tang Y, Xie G, Jia W. Increased intestinal bile acid absorption contributes to age-related cognitive impairment. Cell Rep Med. 2024;5:101543. [PubMed] [DOI] |
| 32. | Dong W, Jia C, Li J, Zhou Y, Luo Y, Liu J, Zhao Z, Zhang J, Lin S, Chen Y. Fisetin Attenuates Diabetic Nephropathy-Induced Podocyte Injury by Inhibiting NLRP3 Inflammasome. Front Pharmacol. 2022;13:783706. [PubMed] [DOI] |
| 33. | Armstrong LE, Guo GL. Role of FXR in Liver Inflammation during Nonalcoholic Steatohepatitis. Curr Pharmacol Rep. 2017;3:92-100. [PubMed] [DOI] |
| 34. | Hosseinkhani F, Heinken A, Thiele I, Lindenburg PW, Harms AC, Hankemeier T. The contribution of gut bacterial metabolites in the human immune signaling pathway of non-communicable diseases. Gut Microbes. 2021;13:1-22. [PubMed] [DOI] |
| 35. | Chen X, Liu M, Tang J, Wang N, Feng Y, Ma H. Research Progress on the Therapeutic Effect of Polysaccharides on Non-Alcoholic Fatty Liver Disease through the Regulation of the Gut-Liver Axis. Int J Mol Sci. 2022;23:11710. [PubMed] [DOI] |
| 36. | Krueger WS, Hilborn ED, Converse RR, Wade TJ. Environmental risk factors associated with Helicobacter pylori seroprevalence in the United States: a cross-sectional analysis of NHANES data. Epidemiol Infect. 2015;143:2520-2531. [PubMed] [DOI] |
| 37. | Xie L, Liu GW, Liu YN, Li PY, Hu XN, He XY, Huan RB, Zhao TL, Guo HJ. Prevalence of Helicobacter pylori infection in China from 2014-2023: A systematic review and meta-analysis. World J Gastroenterol. 2024;30:4636-4656. [PubMed] [DOI] |
| 38. | Wu Y, Zheng Q, Zou B, Yeo YH, Li X, Li J, Xie X, Feng Y, Stave CD, Zhu Q, Cheung R, Nguyen MH. The epidemiology of NAFLD in Mainland China with analysis by adjusted gross regional domestic product: a meta-analysis. Hepatol Int. 2020;14:259-269. [PubMed] [DOI] |
| 39. | Wang T, Xi Y, Raji A, Crutchlow M, Fernandes G, Engel SS, Zhang X. Overall and subgroup prevalence of non-alcoholic fatty liver disease and prevalence of advanced fibrosis in the United States: An updated national estimate in National Health and Nutrition Examination Survey (NHANES) 2011-2018. Ann Hepatol. 2024;29:101154. [PubMed] [DOI] |
学科分类: 胃肠病学和肝病学
手稿来源地: 山东省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C
D级 (一般): 0
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁