修回日期: 2026-02-04
接受日期: 2026-02-25
在线出版日期: 2026-02-28
目前临床对于超声造影鉴别诊断原发性肝癌与转移性肝癌的价值尚不明确, 且缺乏定量分析, 基于此, 本研究试分析超声造影诊断原发性肝癌及肝转移瘤与病理活检一致性.
探讨超声造影(contrast-enhanced ultrasound, CEUS)对原发性肝癌及肝转移瘤的诊断价值, 以期为临床鉴别诊断提供参考.
选取89例湖州市第一人民医院2022-03/2023-12就诊的肝癌患者作为研究对象, 经病理活检结果分为原发性肝癌组(n = 52)、肝转移瘤组(n = 37), 入院后均行CEUS检查, 统计原发性肝癌及肝转移瘤CEUS影像特征, 比较两组CEUS各时间点病灶实质增强强度, 并比较两组CEUS定量参数[峰值强度(peak intensity, PI)、达峰时间(peak time, TTP)、曲线下面积(area under the curve, AUC)]及血清肿瘤标志物[甲胎蛋白(alpha-fetoprotein, AFP)、癌胚抗原(carcinoembryonic antigen, CEA)], 分析CEUS参数与血清肿瘤标志物水平相关性, 并分析CEUS诊断原发性肝癌及肝转移瘤及临床分期与病理活检一致性.
原发性肝癌组病灶达峰强度、病灶达峰后5 s、10 s、30 s、50 s、80 s强度高于肝转移瘤组, 差异具有统计学意义(P<0.05); 原发性肝癌组病灶CEUS定量参数TTP、PI、AUC及血清AFP水平高于肝转移瘤组, 血清CEA低于肝转移瘤组, 差异具有统计学意义(P<0.05); 经Pearson相关性分析结果显示, CEUS定量参数TTP、PI、AUC与血清AFP水平呈正相关, 与血清CEA水平呈负相关(P<0.05); CEUS对原发性肝癌诊断敏感度为90.38%(47/52), 特异度为94.59%(35/37), 准确度为92.13%(82/89); CEUS诊断原发性肝癌、肝转移瘤与病理诊断结果一致性Kappa值为0.839(P<0.05); CEUS诊断原发性肝癌临床分期结果与病理诊断结果一致性Kappa值为0.820, 准确度为87.23%(P<0.05).
CEUS诊断原发性肝癌及肝转移瘤与病理活检具有高度一致性, 为临床鉴别诊断、评估临床分期提供参考依据, 以针对性制定相应干预方案.
核心提要: 目前临床对于超声造影鉴别诊断原发性肝癌与转移性肝癌的价值尚不明确, 且缺乏定量分析, 基于此, 本研究试分析超声造影诊断原发性肝癌及肝转移瘤与病理活检一致性.
引文著录: 周振江, 邓弼云. 超声造影原发性肝癌及肝转移瘤与病理活检一致性研究. 世界华人消化杂志 2026; 34(2): 130-137
Revised: February 4, 2026
Accepted: February 25, 2026
Published online: February 28, 2026
At present, the clinical value of contrast-enhanced ultrasound (CEUS) in the differential diagnosis of primary liver cancer and metastatic liver cancer is still unclear, and quantitative analysis is lacking. This study attempted to analyze the consistency between CEUS and pathological biopsy in the diagnosis of primary liver cancer and liver metastases.
To investigate the consistency of CEUS and pathological biopsy in the diagnosis of primary liver cancer and liver metastases, in order to provide reference for early clinical differential diagnosis and targeted intervention.
A total of 89 patients with liver cancer who received medical treatment at the First People's Hospital of Huzhou City from March 2022 to December 2023 were prospectively selected and divided into a primary liver cancer group (n = 52) and a liver metastasis group (n = 37) according to pathological biopsy results. CEUS imaging features for primary liver cancer and liver metastasis were analyzed after admission. The enhancement intensity of the focal lesion was compared between the two groups at each time point of CEUS. Quantitative parameters of CEUS [peak time (TTP), peak intensity (PI), and area under the curve (AUC)] and serum tumor markers [alpha-fetoprotein (AFP) and carcinoembryonic antigen (CEA)] were compared between the two groups, and the correlation between CEUS parameters and serum tumor markers was analyzed. The consistency between CEUS and and pathological biopsy in staging primary liver cancer and liver metastases was analyzed.
The PI, as well as the values at 5 s, 10 s, 30 s, 50 s, and 80 s after peaking in the primary liver cancer group were significantly higher than those of the liver metastasis group (P < 0.05). The quantitative parameters TTP, PI, AUC, and serum AFP levels in the primary liver cancer group were significantly higher than those of the liver metastasis group, and serum CEA levels were significantly lower than those of the liver metastasis group (P < 0.05). Pearson correlation analysis showed that the quantitative parameters TTP, PI, and AUC were positively correlated with serum AFP level, and negatively correlated with serum CEA level (P < 0.05). The sensitivity, specificity, and accuracy of CEUS for diagnosing primary liver cancer were 90.38% (47/52), 94.59% (35/37), and 92.13% (82/89), respectively. The Kappa value of CEUS in the diagnosis of primary liver cancer and liver metastasis was 0.839 (P < 0.05). The Kappa value of CEUS and pathological biopsy in staging primary liver cancer was 0.820, with an accuracy of 87.23% (P < 0.05).
CEUS demonstrates high consistency with pathological biopsy in diagnosing primary liver cancer and liver metastases, offering a valuable reference for early differential diagnosis and clinical staging to guide timely intervention.
- Citation: Zhou ZJ, Deng BY. Consistency between contrast-enhanced ultrasound imaging and pathological biopsy in diagnosis of primary liver cancer and liver metastases. Shijie Huaren Xiaohua Zazhi 2026; 34(2): 130-137
- URL: https://www.wjgnet.com/1009-3079/full/v34/i2/130.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v34.i2.130
原发性肝癌与转移性肝癌为临床常见肝脏肿瘤, 其中原发性肝癌多发生于有慢性肝病病史基础患者且为单发, 而肝转移瘤多发生于有原发性非肝脏恶性肿瘤者且为多发, 但部分原发性肝癌也可发生于正常肝脏背景中, 肝转移瘤也可能为孤立性, 因此临床对于原发性肝癌及肝转移瘤鉴别诊断存在一定难度, 从而影响早期治疗[1-3]. 故积极探讨原发性肝癌及肝转移瘤早期有效鉴别诊断方案具有重大意义. 超声造影目前已用于肿瘤早期评估诊断中, 可反映各个组织血流灌注状态并评估其病变情况, 且随超声仪器改善及第二代超声微泡造影剂的应用, 超声造影已逐渐用于肝脏占位性病变诊断中[4-6]. 但目前临床对于超声造影鉴别诊断原发性肝癌与转移性肝癌的价值尚不明确, 且缺乏定量分析. 基于此, 本研究试分析超声造影诊断原发性肝癌及肝转移瘤与病理活检一致性.
经湖州市第一人民医院伦理委员会审核批准, 选取89例湖州市第一人民医院2022-03/2023-12就诊的肝癌患者作为研究对象, 经病理活检结果分为原发性肝癌组(n = 52)、肝转移瘤组(n = 37), 其中肝转移瘤原发病灶: 结肠癌12例, 胃癌10例, 肺癌8例, 乳腺癌7例. 两组年龄、性别、体质量指数、病灶平均大小、合并高血压、高血脂症、糖尿病均衡可比(P>0.05). 见表1.
| 组别 | 例数 | 性别(男/女) | 年龄(mean±SD, 岁) | BMI(mean±SD, kg/m2) | 病灶平均大小(mean±SD, cm) | 基础疾病 | ||
| 高血压 | 高血脂症 | 糖尿病 | ||||||
| 原发性肝癌组 | 52 | 31/21 | 61.74±4.86 | 23.57±1.06 | 5.25±1.36 | 22(42.31) | 15(28.85) | 7(13.46) |
| 肝转移瘤组 | 37 | 22/15 | 62.15±5.13 | 23.72±1.03 | 5.18±1.29 | 12(32.43) | 8(21.62) | 3(8.11) |
| χ2/t | 0.042 | 0.383 | 0.666 | 0.244 | 0.893 | 0.589 | 0.621 | |
| P值 | 0.838 | 0.702 | 0.507 | 0.807 | 0.345 | 0.443 | 0.431 | |
纳入标准: 所有患者均经影像学检查、病理组织活检确诊为原发性肝癌或肝转移瘤; 可接受超声造影检查; 患者及家属知晓本研究, 并签订同意书.
排除标准: 合并其他肝脏疾病、恶性肿瘤者; 孕妇及未成年人; 入院前已接受相关抗肿瘤治疗者; 合并其他重大脏器功能障碍; 合并活动性感染、自身免疫性疾病者; 合并本研究检查绝对禁忌症者; 合并精神障碍或检查依从性较差.
超声造影检查: 均采用Philips iU22型超声诊断仪检查, 探头频率为3.5-5.0 MHz, 造影剂为Bracco声诺维. 引导患者处仰卧位, 先行常规超声扫描, 记录病灶位置、数目、大小、回声等信息; 切面至超声造影模式, 调节机械指数至0.05-0.10, 经患者肘静脉后注射2.4 mL造影剂, 随后迅速注射5 mL生理盐水冲管, 注射时同时启动内置计时器, 观察病灶动脉灌注情况, 所有图像均记录于超声仪硬盘, 由2名超声医师分析存储的动态图像, 观察病灶的增强模式.
图像分析: 逐帧回放存储的动态超声造影图像, 通过后台软件获取时间-强度曲线, 将取样框置于感兴趣区高回声部分, 获取超声造影定量参数[达峰时间(peak time, TTP)、峰值强度(peak intensity, PI)、曲线下面积(area under the curve, AUC)].
血清标志物检测: 均采集入院时外周静脉血3 mL, 经离心半径8 cm、3500 r/min离心10 min后, 分离血清保存待测. 采用化学发光免疫分析法测定血清癌胚抗原(carcinoembryonic antigen, CEA)水平(正常值范围: 0-5 μg/L)、甲胎蛋白(alpha-fetoprotein, AFP)水平(正常值范围: 0-20 μg/L), 试剂盒购于上海科艾博生物有限公司. 所有操作均严格按照试剂盒及仪器相关说明进行.
临床分期标准: 根据国际抗癌联盟与美国肿瘤联合会联合制定的TNM分期法进行分期, 其中Ⅰ期: 肿瘤局限于肝脏内, 无淋巴结转移及远端转移现象; Ⅱ期: 肿瘤出现局部淋巴结转移, 但未出现远端转移现象; Ⅲ期: 肿瘤出现肺、脑等远端转移; Ⅳ期: 肿瘤出现腹腔、淋巴结等远端转移.
(1)分析原发性肝癌及肝转移瘤超声造影影像学特征; (2)比较两组超声造影各时间点病灶实质增强强度; (3)比较两组超声造影定量参数及血清肿瘤标志物水平; (4)分析超声造影定量参数与血清肿瘤标志物水平相关性; (5)基于超声造影定量参数构建诊断模型, 分析超声造影诊断原发性肝癌及肝转移瘤与病理活检一致性; 和(6)分析超声造影诊断原发性肝癌临床分期与病理活检一致性.
统计学处理 采用SPSS 28.0软件处理分析相关数据, 符合正态分布的计量资料用(mean±SD)表示, 两组间比较采用独立样本t检验, 计数资料用n(%)表示, 两组间比较行χ2检验, Pearson行相关性分析, 诊断价值分析采用受试者工作特征曲线, 采用Kappa值进行一致性分析, 其中Kappa值<0.4为差, 0.4-0.75为良好, >0.75为优, 默认双侧检验, α = 0.05.
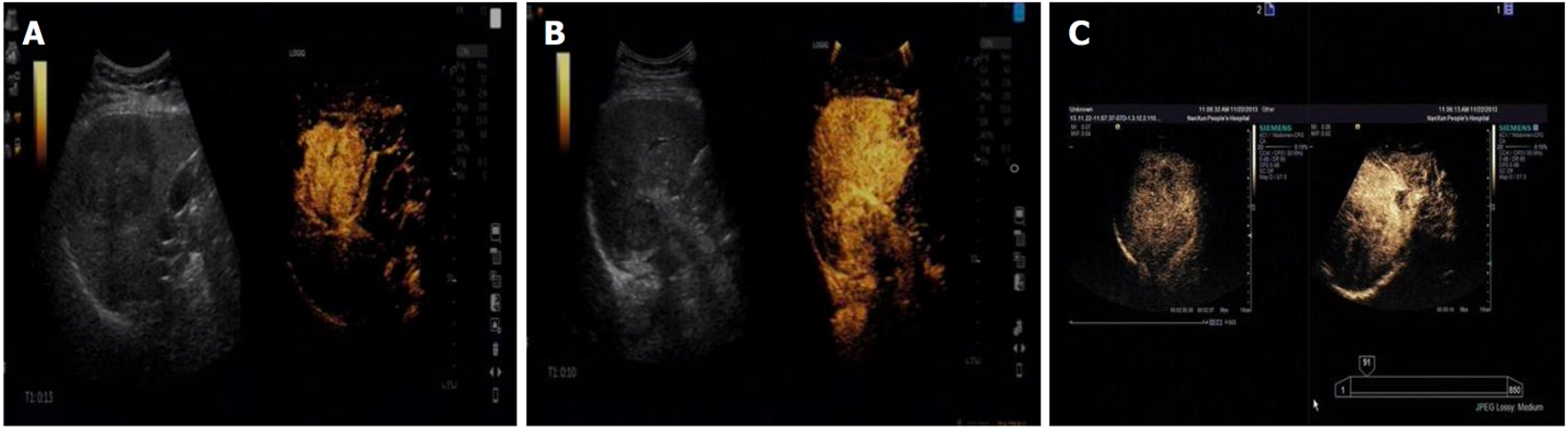
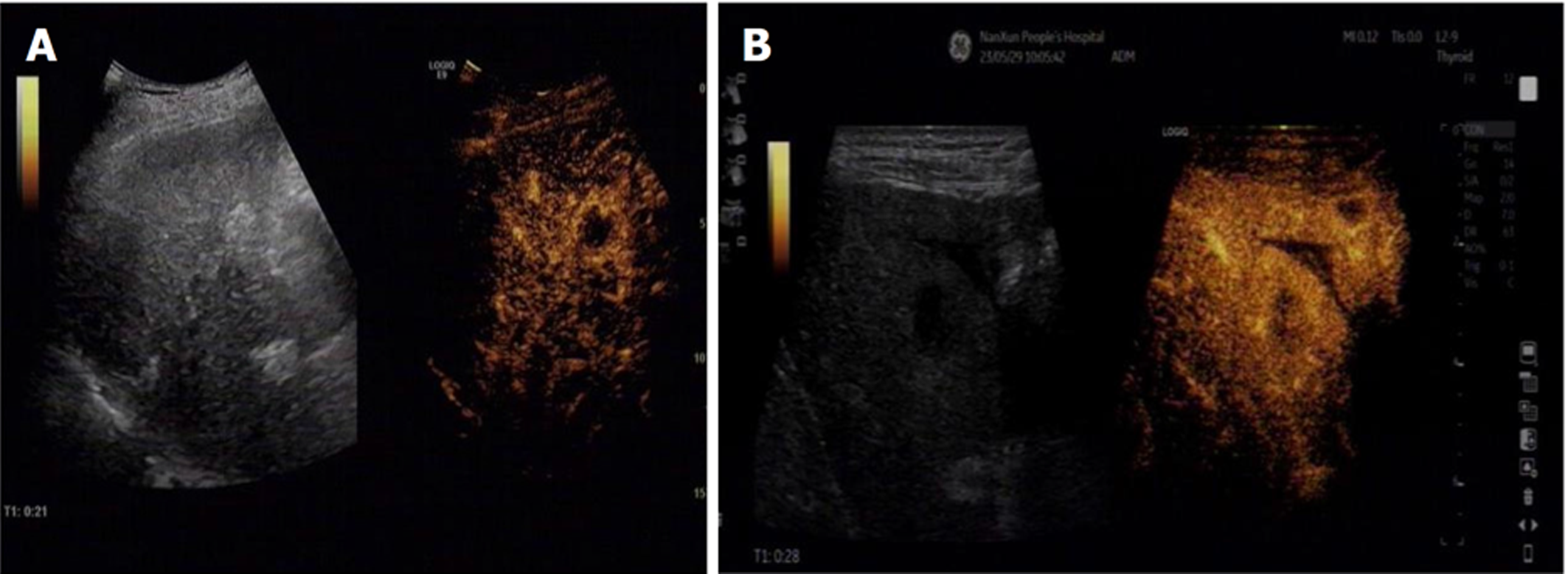
经超声造影检查结果显示, 原发性肝癌动脉相早期呈整体增强, 呈"快进快出"型表现, 边界多不规则, 具有周围血管围绕征, 肿瘤内血流信号杂乱, 肿瘤后方回声无明显变化, 少数后方回声轻度增强; 而肝转移瘤超声造影特征主要呈强回声、不规则形状、快速显影、血供丰富等, 动脉相早期大部分呈整体增强, 周边呈厚圈状增强, 中心部位无增强, 廓清后均呈"黑洞"表现. 见图1和图2.
原发性肝癌组病灶达峰强度、病灶达峰后5 s、10 s、30 s、50 s、80 s强度高于肝转移瘤组(P<0.05). 见表2.
| 组别 | 例数 | 达峰 | 病灶达峰后5 s | 病灶达峰后10 s | 病灶达峰后30 s | 病灶达峰后50 s | 病灶达峰后80 s |
| 原发性肝癌组 | 52 | 31.84±3.25 | 29.32±2.64 | 26.54±2.39 | 21.84±2.59 | 19.38±2.42 | 15.63±2.19 |
| 肝转移瘤组 | 37 | 28.19±3.06 | 20.74±2.31 | 19.24±2.09 | 14.32±1.86 | 12.74±2.15 | 10.24±1.58 |
| t | 5.349 | 15.902 | 14.948 | 15.907 | 13.353 | 12.781 | |
| P值 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 |
原发性肝癌组病灶超声造影定量参数TTP、PI、AUC及血清AFP水平高于肝转移瘤组, 血清CEA低于肝转移瘤组(P<0.05). 见表3.
| 组别 | 例数 | TTP(s) | PI(dB) | AUC | AFP(μg/L) | CEA(μg/L) |
| 原发性肝癌组 | 52 | 15.84±1.79 | 46.93±5.12 | 2315.94±85.93 | 3584.19±193.48 | 12.93±2.52 |
| 肝转移瘤组 | 37 | 12.73±1.48 | 39.25±4.38 | 1259.38±51.74 | 48.41±5.82 | 83.96±7.15 |
| t | 8.665 | 7.397 | 66.627 | 110.941 | 66.214 | |
| P值 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 |
经Pearson相关性分析结果显示, 超声造影定量参数TTP、PI、AUC与血清AFP水平呈正相关, 与血清CEA水平呈负相关(P<0.05). 见表4.
| 指标 | TTP(s) | PI(dB) | AUC | |||
| r值 | P值 | r值 | P值 | r值 | P值 | |
| AFP(μg/L) | 0.762 | <0.001 | 0.748 | <0.001 | 0.831 | <0.001 |
| CEA(μg/L) | -0.739 | <0.001 | -0.718 | <0.001 | -0.809 | <0.001 |
基于超声造影定量参数构建诊断模型, 经超声造影检查结果显示, 共检出原发性肝癌49例, 肝转移瘤40例. 以病理诊断结果为"金标准", 超声造影对原发性肝癌诊断敏感度为90.38%(47/52), 特异度为94.59%(35/37), 准确度为92.13%(82/89); 超声造影诊断原发性肝癌、肝转移瘤与病理诊断结果一致性Kappa值为0.839(P<0.05). 见表5.
| 病理诊断 | 超声造影 | 合计 | Kappa值 | P值 | 95%CI | |
| 原发性肝癌 | 肝转移瘤 | |||||
| 原发性肝癌 | 47 | 5 | 52 | 0.839 | <0.001 | 0.633-1.047 |
| 肝转移瘤 | 2 | 35 | 37 | |||
| 合计 | 49 | 40 | 89 | |||
超声造影检出的47例原发性肝癌患者中, 经病理诊断结合肿瘤转移、侵袭情况进行临床分期, 结果显示: Ⅰ期9例, Ⅱ期18例, Ⅲ期13例, Ⅳ期7例; 经超声造影诊断结果显示: Ⅰ期7例, Ⅱ期20例, Ⅲ期13例, Ⅳ期7例; 超声造影诊断原发性肝癌临床分期结果与病理诊断结果一致性Kappa值为0.820, 准确度为87.23%(P<0.05). 见表6.
| 病理诊断 | 超声造影 | 合计 | Kappa值 | P值 | 95%CI | |||
| Ⅰ期 | Ⅱ期 | Ⅲ期 | Ⅳ期 | |||||
| Ⅰ期 | 7 | 2 | 0 | 0 | 9 | 0.820 | <0.001 | 0.643-1.012 |
| Ⅱ期 | 0 | 17 | 1 | 0 | 18 | |||
| Ⅲ期 | 0 | 1 | 11 | 1 | 13 | |||
| Ⅳ期 | 0 | 0 | 1 | 6 | 7 | |||
| 合计 | 7 | 20 | 13 | 7 | 47 | |||
另选取68例2022-03/2023-12就诊的肝癌患者作为外部验证数据, 经病理活检结果分为原发性肝癌组(n = 42)、肝转移瘤组(n = 26), 基于超声造影定量参数构建的诊断模型诊断结果显示, 敏感度为90.47%(38/42), 特异度为92.31%(24/26), 且经一致性分析显示, 与临床实际的一致性较高(Kappa值 = 0.841, 95%CI: 0.596-1.086).
原发性肝癌及肝转移瘤为临床常见肝内恶性肿瘤, 而不同肝内肿瘤临床治疗方案相应不同, 早期有效鉴别诊断、明确肿瘤分期, 对于患者制定治疗方案、改善预后均具有重大意义[7,8]. 目前临床对于肝内恶性肿瘤多通过影像学特征结合以往病史进行初步诊断, 其中在肝炎、肝硬化等基础上发现肝内占位性病灶者则优先考虑为原发性肝癌, 而存在原发性恶性肿瘤病史、肝内多发病灶者则优先考虑为肝转移瘤, 但在无肝炎、肝硬化、恶性肿瘤病史情况下, 临床鉴别诊断存在一定难度[9,10]. 因此, 积极探讨原发性肝癌及肝转移瘤有效鉴别方案至关重要.
超声检查已广泛应用于肝脏占位性病变诊断中, 为临床筛查肝脏恶性肿瘤的首选方案, 但原发性肝癌及肝转移瘤的常规二维超声声像图表现存在交叉, 部分难以作出准确鉴别诊断[11]. 超声造影通过注射造影剂进行连续扫查, 可实时观察病灶与肝实质血流灌注过程, 有效区分肝脏血流灌注时相, 有助于准确评估病灶血供特点, 且可通过后台自动追踪对比软件, 获取PI等定量参数, 从而提高诊断准确度及客观性[12-14]. 本研究结果显示, 两组超声造影各时间点病灶实质增强强度及超声造影定量参数比较存在显著差异, 提示临床可通过超声造影检查结合定量参数早期评估诊断原发性肝癌及肝转移瘤. 报道显示[15-17], 超声造影可提高肝脏微小病灶检出率, 准确反映、呈现病变组织血流灌注情况, 而不同肝脏肿瘤血供特征不同, 超声造影增强模式相应不同, 因此可通过超声造影影像特征进行初步鉴别, 但由于部分肝转移瘤超声造影表现类似于原发性肝癌增强模式, 如部分富血供肝转移瘤与高分化肝细胞癌相似, 导致单纯通过影像特征鉴别诊断存在混淆. 而本研究通过结合超声造影定量参数进行分析, 根据超声定量参数TTP、PI等可有效评估病灶血流灌注情况, 由于肝脏为富血流器官, 不同肝脏肿瘤组织中造影剂随血液循环到达肿瘤组织的时间不同, 而原发性肝癌组织血流量相较于肝转移瘤较高, 导致PI、AUC等参数水平上调[18-20]. 超声造影定量参数中TTP反映造影剂在病灶微血管内的灌注速度, 肿瘤血管由肝动脉异常增生形成, 血管分支复杂、血流路径相对较长, 因此TTP显著高于肝转移瘤; PI指造影剂在病灶内达到的最大增强信号强度, 肝细胞癌因促血管生成因子高表达, 肿瘤间质内形成大量功能性微血管, 导致造影剂最大聚集量高, PI随之升高; 而AUC可综合反映造影剂在病灶内的总灌注量与灌注持续时间, 原发性肝癌的微血管覆盖范围广, 且血流储备能力强, 造影剂在病灶内的停留时间长、总灌注量大, 导致AUC更高. 另有研究表明[21,22], 通过计算超声造影各时间点病灶强度下降程度, 可半定量分析原发性肝癌与肝转移瘤的下降趋势, 可弥补时间-强度曲线无法拟合曲线下降支的缺陷, 提高诊断准确性.
血清肿瘤标志物为临床鉴别诊断原发性肝癌及肝转移瘤的主要方案, 其中AFP为一种单链多肽糖蛋白, 可作用于肝癌细胞或间接抑制免疫系统, 促进肝癌的发生、发展, 而CEA为一种瘤胎糖蛋白, 正常人血清CEA水平含量较低, 但失去极性的癌细胞可分泌大量CEA进入血液、淋巴液中, 导致血清CEA水平显著升高[23-25]. 本研究结果显示, 两组血清AFP、CEA水平存在显著差异, 经相关性分析显示, 超声造影定量参数与血清AFP、CEA水平均具有相关性, 进一步说明超声造影定量参数对原发性肝癌及肝转移瘤的评估诊断价值. 此外, 本研究结果还发现, 超声造影对原发性肝癌诊断准确度为92.13%, 对于原发性肝癌、肝转移瘤与病理诊断结果一致性Kappa值为0.839, 对于原发性肝癌临床分期结果与病理诊断结果一致性Kappa值为0.820, 具有高度一致性, 提示临床可通过超声造影鉴别诊断原发性肝癌、肝转移瘤. 范懿等[26]学者研究表明, 基于彩色多普勒超声瘤内、瘤周血流信号鉴别诊断原发性肝癌与肝转移瘤, 其诊断准确度为89.47%, 一致性Kappa值为0.790, 而本研究超声造影的鉴别准确度为92.13%, 一致性Kappa值为0.839, 均优于彩色多普勒超声. 游斌等学者研究发现, 动态对比增强磁共振成像(magnetic resonance imaging, MRI)对原发性肝癌与肝转移瘤的诊断结果与术后病理具有较高一致性(Kappa = 0.893), 本研究略低于动态对比增强MRI, 进一步证实其对原发性肝癌、肝转移瘤的鉴别诊断价值. 从临床应用角度分析, 超声造影操作简便、价格低廉, 适用于基层医院推广应用, 可为临床术中精准定位病灶提供依据, 且可结合血清肿瘤标志物进行鉴别诊断, 为临床制定干预方案提供参考.
综上所述, 超声造影对于原发性肝癌、肝转移瘤具有较高鉴别诊断价值, 临床可通过其定量参数辅助诊断, 有助于临床评估病情、制定干预方案. 但本研究仍存在一定局限性, 如本研究选取样本量较少, 可能会影响研究结果的代表性和可靠性, 且超声造影检查可能受操作者经验、仪器设备等因素影响, 可能会对研究结果产生一定的偏差, 后续可进一步扩大样本量并验证医师诊断结果一致性, 以提高结果准确性.
部分原发性肝癌也可发生于正常肝脏背景中, 肝转移瘤也可能为孤立性, 因此临床对于原发性肝癌及肝转移瘤鉴别诊断存在一定难度, 从而影响早期治疗. 故积极探讨原发性肝癌及肝转移瘤早期有效鉴别诊断方案具有重大意义.
超声造影目前已用于肿瘤早期评估诊断中, 可反映各个组织血流灌注状态并评估其病变情况, 已逐渐用于肝脏占位性病变诊断中, 目前临床对于超声造影鉴别诊断原发性肝癌与转移性肝癌的价值尚不明确, 且缺乏定量分析.
超声造影对原发性肝癌及肝转移瘤的诊断价值, 以期为临床鉴别诊断提供参考.
选取89例就诊的肝癌患者作为研究对象, 分为原发性肝癌组、肝转移瘤组, 行超声造影(contrast-enhanced ultrasound, CEUS)检查, 分析CEUS参数与血清肿瘤标志物水平相关性, 并分析CEUS诊断原发性肝癌及肝转移瘤及临床分期与病理活检一致性.
结果显示, 两组血清[甲胎蛋白(alpha-fetoprotein, AFP)、癌胚抗原(carcinoembryonic antigen, CEA)]水平存在显著差异, 经相关性分析显示, 超声造影定量参数与血清AFP、CEA水平均具有相关性, 进一步说明超声造影定量参数对原发性肝癌及肝转移瘤的评估诊断价值.
CEUS诊断原发性肝癌及肝转移瘤与病理活检具有高度一致性, 为临床鉴别诊断、评估临床分期提供参考依据, 以针对性制定相应干预方案.
超声造影操作简便、价格低廉, 适用于基层医院推广应用, 可为临床术中精准定位病灶提供依据, 且可结合血清肿瘤标志物进行鉴别诊断, 为临床制定干预方案提供参考.
| 1. | Rumgay H, Arnold M, Ferlay J, Lesi O, Cabasag CJ, Vignat J, Laversanne M, McGlynn KA, Soerjomataram I. Global burden of primary liver cancer in 2020 and predictions to 2040. J Hepatol. 2022;77:1598-1606. [PubMed] [DOI] |
| 2. | Xian L, Zhao P, Chen X, Wei Z, Ji H, Zhao J, Liu W, Li Z, Liu D, Han X, Qian Y, Dong H, Zhou X, Fan J, Zhu X, Yin J, Tan X, Jiang D, Yu H, Cao G. Heterogeneity, inherent and acquired drug resistance in patient-derived organoid models of primary liver cancer. Cell Oncol (Dordr). 2022;45:1019-1036. [PubMed] [DOI] |
| 3. | Li X, Ramadori P, Pfister D, Seehawer M, Zender L, Heikenwalder M. The immunological and metabolic landscape in primary and metastatic liver cancer. Nat Rev Cancer. 2021;21:541-557. [PubMed] [DOI] |
| 6. | Squires JH, Fetzer DT, Dillman JR. Practical Contrast Enhanced Liver Ultrasound. Radiol Clin North Am. 2022;60:717-730. [PubMed] [DOI] |
| 7. | De Siervi S, Turato C. Liver Organoids as an In Vitro Model to Study Primary Liver Cancer. Int J Mol Sci. 2023;24:4529. [PubMed] [DOI] |
| 8. | Zuo Q, Park NH, Lee JK, Madak Erdogan Z. Liver Metastatic Breast Cancer: Epidemiology, Dietary Interventions, and Related Metabolism. Nutrients. 2022;14:2376. [PubMed] [DOI] |
| 9. | Chen Z, Zhang G, Ren X, Yao Z, Zhou Q, Ren X, Chen S, Xu L, Sun K, Zeng Q, Kuang M, Kuang DM, Peng S. Cross-talk between Myeloid and B Cells Shapes the Distinct Microenvironments of Primary and Secondary Liver Cancer. Cancer Res. 2023;83:3544-3561. [PubMed] [DOI] |
| 10. | Shi JF, Cao M, Wang Y, Bai FZ, Lei L, Peng J, Feletto E, Canfell K, Qu C, Chen W. Is it possible to halve the incidence of liver cancer in China by 2050? Int J Cancer. 2021;148:1051-1065. [PubMed] [DOI] |
| 11. | 袁 焕勤, 刘 高升, 袁 振林, 等. 彩色多普勒超声评估复发性肝癌经导管肝动脉化疗栓塞术患者临床预后价值. 中国现代普通外科进展. 2023;26:634-636, 640. [DOI] |
| 12. | Como G, Montaldo L, Baccarani U, Lorenzin D, Zuiani C, Girometti R. Contrast-enhanced ultrasound applications in liver transplant imaging. Abdom Radiol (NY). 2021;46:84-95. [PubMed] [DOI] |
| 13. | Piscaglia F, Sansone V, Tovoli F. Contrast-enhanced ultrasound of the liver in colorectal cancer: A useful tool in the right patient. J Hepatol. 2021;74:272-273. [PubMed] [DOI] |
| 14. | Dong Y, Koch JBH, Löwe AL, Christen M, Wang WP, Jung EM, Mohaupt MG, Dietrich CF. VueBox® for quantitative analysis of contrast-enhanced ultrasound in liver tumors1. Clin Hemorheol Microcirc. 2022;80:473-486. [PubMed] [DOI] |
| 15. | Dong Y, Wang WP, Lee WJ, Meloni MF, Clevert DA, Chammas MC, Tannapfel A, Forgione A, Piscaglia F, Dietrich CF. Contrast-Enhanced Ultrasound Features of Histopathologically Proven Hepatocellular Carcinoma in the Non-cirrhotic Liver: A Multicenter Study. Ultrasound Med Biol. 2022;48:1797-1805. [PubMed] [DOI] |
| 16. | Liu W, Zhang ZY, Yin SS, Yan K, Xing BC. Contrast-Enhanced Intraoperative Ultrasound Improved Sensitivity and Positive Predictive Value in Colorectal Liver Metastasis: a Systematic Review and Meta-Analysis. Ann Surg Oncol. 2021;28:3763-3773. [PubMed] [DOI] |
| 18. | Vidili G, Arru M, Solinas G, Calvisi DF, Meloni P, Sauchella A, Turilli D, Fabio C, Cossu A, Madeddu G, Babudieri S, Zocco MA, Iannetti G, Di Lembo E, Delitala AP, Manetti R. Contrast-enhanced ultrasound Liver Imaging Reporting and Data System: Lights and shadows in hepatocellular carcinoma and cholangiocellular carcinoma diagnosis. World J Gastroenterol. 2022;28:3488-3502. [PubMed] [DOI] |
| 20. | Sawatzki M, Güller U, Güsewell S, Husarik DB, Semela D, Brand S. Contrast-enhanced ultrasound can guide the therapeutic strategy by improving the detection of colorectal liver metastases. J Hepatol. 2021;74:419-427. [PubMed] [DOI] |
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C, C, C
D级 (一般): D
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁