修回日期: 2026-02-20
接受日期: 2026-02-25
在线出版日期: 2026-02-28
现有研究明确消化道重建方式、术前营养状态等与胃癌术后营养不良相关, 但多采用Logistic回归等传统统计方法构建预测模型, 难以解析多因素复杂交互效应; 且营养不良倡议(global leadership initiative on malnutrition, GLIM)诊断标准与胃癌等肿瘤患者预后的关联性仍需进一步探究证实.
基于贝叶斯网络(tree augmented naive Bayes, TAN)模型分析胃癌根治术后患者营养不良的相关因素及其对预后的影响.
选取2024-03/2025-01杭州市余杭区第二人民医院246例胃癌患者, 根据GLIM标准进行营养不良诊断, 采用Logistics回归和TAN模型分析营养不良发生的影响因素及各因素间的关系. 通过Kaplan-Meier及Cox回归分析营养不良对预后的影响, 受试者工作特征曲线评价其对胃癌根治术后生存率的预测价值.
Logistic回归分析显示, 全胃切除、营养不良风险筛查2002(NRS2002)≥3分、术后辅助化疗、术前营养不良、血清瘦素(Leptin)是胃癌根治术后营养不良的危险因素, 白蛋白、血清食欲素A(Orexin A)是其保护因素(P<0.05); 基于15个临床病理学因素构建的TAN模型曲线下面积(area under the curve, AUC)为0.807(95%CI: 0.752-0.854), 基于单因素分析构建的TAN模型AUC为0.828(95%CI: 0.775-0.873), 基于Logistic分析结果的7个影响因素构建的TAN模型AUC为0.866(95%CI: 0.817-0.906); Kaplan Meier显示, 与营养不良患者相比, 术后营养正常患者预后更好(P<0.05), Cox回归分析显示GLIM标准中非自主体重减轻、低身体质量指数、肌肉质量减少、C反应蛋白/白蛋白比值是影响胃癌根治术后预后的重要因素(P<0.05), 基于GLIM标准的营养不良预测胃癌根治术后患者预后的AUC为0.930(95%CI: 0.890-0.958), 敏感性、特异性分别为88.76%、87.01%.
全胃切除、NRS2002≥3分、术后辅助化疗、术前营养不良、白蛋白、血清Orexin A、血清Leptin是胃癌根治术后营养不良的影响因素, 而基于GLIM诊断标准的营养不良对生存预后有重要影响, 且TAN构建的预测模型能反映胃癌根治术后营养不良的风险.
核心提要: 本研究首次将贝叶斯网络模型引入胃癌根治术后营养分析领域, 系统解析多维影响因素与营养不良的关系以及其对预后的影响, 旨在为个体化营养干预方案的制定提供理论依据, 为复杂临床问题因果推论提供方法学参考.
引文著录: 姚智刚, 鲁雅儿. 基于贝叶斯网络模型分析胃癌根治术后患者营养不良的相关因素及与预后的关联性分析. 世界华人消化杂志 2026; 34(2): 121-129
Revised: February 20, 2026
Accepted: February 25, 2026
Published online: February 28, 2026
Although existing studies have confirmed that digestive tract reconstruction, preoperative nutritional status, and other factors are associated with postoperative malnutrition in gastric cancer patients, most have used traditional statistical methods such as Logistic regression to construct prediction models, which are inadequate for analyzing complex interactions among multiple factors. Furthermore, the correlation between the global leadership initiative on malnutrition (GLIM) criteria for malnutrition and the prognosis of patients with gastric cancer and other tumors remains to be further investigated and verified.
To analyze the related factors of malnutrition in patients after radical resection of gastric cancer and its impact on prognosis based on the tree augmented naive Bayes (TAN) model.
A total of 246 patients with gastric cancer who underwent radical resection from March 2024 to January 2025 in our hospital were selected, and malnutrition was diagnosed according to the GLIM criteria. Logistic regression and TAN models were used to analyze the influencing factors that contribute to malnutrition. The impact of malnutrition on prognosis was analyzed using Kaplan-Meier and Cox regression analysis, and the predictive value of malnutrition for survival after radical resection of gastric cancer was evaluated using receiver operating characteristic curve analysis.
Logistic regression analysis showed that total gastrectomy, NRS2002 score ≥ 3, postoperative adjuvant chemotherapy, preoperative malnutrition, and serum leptin were risk factors for malnutrition after radical resection of gastric cancer, while albumin and serum orexin A were protective factors (P < 0.05). The area under the curve (AUC) values of the TAN model constructed based on 15 clinical and pathological factors, the TAN model constructed based on univariate analysis results, and the TAN model constructed based on the results of logistic analysis were 0.807 [95% confidence interval (CI): 0.752-0.854], 0.828 (95%CI: 0.775-0.873), and 0.866 (95%CI: 0.817-0.906), respectively. Kaplan-Meier survial analysis showed that patients with normal postoperative nutrition had a better prognosis compared with malnourished patients (P < 0.05). Cox regression analysis showed that non-voluntary weight loss, low body mass index, reduced muscle mass, and C-reactive protein/albumin ratio in the GLIM criteria were important factors affecting the prognosis of patients after radical resection for gastric cancer (P < 0.05). The AUC of the GLIM criteria for predicting the prognosis of patients after radical resection for gastric cancer was 0.930 (95%CI: 0.890-0.958), with a sensitivity and specificity of 88.76% and 87.01%, respectively.
Total gastrectomy, NRS2002 score ≥ 3, postoperative adjuvant chemotherapy, preoperative malnutrition, albumin, serum orexin A, and serum leptin are factors affecting malnutrition after radical resection of gastric cancer. Malnutrition diagnosed based on the GLIM diagnostic criteria has a significant impact on survival prognosis, and the prediction model constructed by TAN can reflect the risk of malnutrition in patients after radical resection of gastric cancer.
- Citation: Yao ZG, Lu YE. Identification of risk factors for malnutrition based on Bayesian network model and analysis of correlation of malnutrition with prognosis in patients after radical resection of gastric cancer. Shijie Huaren Xiaohua Zazhi 2026; 34(2): 121-129
- URL: https://www.wjgnet.com/1009-3079/full/v34/i2/121.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v34.i2.121
核心提要: 本研究首次将贝叶斯网络模型引入胃癌根治术后营养分析领域, 系统解析多维影响因素与营养不良的关系以及其对预后的影响, 旨在为个体化营养干预方案的制定提供理论依据, 为复杂临床问题因果推论提供方法学参考.
胃癌是临床高发恶性肿瘤, 根治切除术是其主要治疗手段, 据统计[1], 术后营养不良发生率高达40%-87%, 会增加并发症风险, 影响远期生存. 尽管现有研究已明确消化道重建方式、术前营养状态等因素与术后营养不良相关, 但多采用Logistic回归等传统统计方法构建风险预测模型, 难以解析多因素间的复杂交互效应[2,3]. 此外, 近年营养不良倡议(global leadership initiative on malnutrition, GLIM)标准指出营养不良诊断需满足至少一个病因和一种表现型标准, 然而GLIM标准与胃癌及其他肿瘤患者预后的关联性仍需进一步探究与证实. 近年来, 贝叶斯网络(tree augmented naive Bayes, TAN)因其在处理多变量、不确定性非线性关系和可视化因果推理方面的诸多优势, 逐渐被用于医疗领域的数据分析[4,5]. 然而, TAN模型在胃癌术后营养状况研究中的应用仍鲜有报道. 因此, 本研究首次将TAN模型引入胃癌根治术后营养分析领域, 系统解析多维影响因素与营养不良的关系以及其对预后的影响, 旨在为个体化营养干预方案的制定提供理论依据, 为复杂临床问题因果推论提供方法学参考.
研究对象: 选取2024-03/2025-01杭州市余杭区第二人民医院246例胃癌患者, 纳入标准: 病理确诊胃癌并行根治切除术; 年龄≥18岁, 能配合术后随访及营养评估; 临床数据及术后随访数据完整. 排除标准: 合并其他严重慢性疾病或恶性肿瘤者; 姑息治疗或非根治性手术者; 术后严重并发症或短期死亡者. 依据样本量估算方法, 样本量可取自变量数的10-20倍, 本研究共15个变量, 又考虑10%的无效率, 计算样本量范围为165-330例.
1.2.1 临床资料收集: 由2名培训合格的研究人员经医院系统查阅患者病历信息, 包括病史、病理类型、性别、临床分期、营养不良风险筛查2002(NRS2002)评分、年龄、术前营养不良等基础资料以及手术切除范围、术后辅助化疗情况等.
1.2.2 实验室指标检测: 首次入院时采集患者静脉血3 mL, 以3000 r/min、10 cm半径离心15 min, 取上层清液, 溴甲酚绿法检测白蛋白(试剂盒货号: NM-W-1108), 双缩脲法检测总蛋白(试剂盒货号: TP-1001), 氰化高铁血红蛋白法检测血红蛋白(试剂盒货号: HB-2001), 酶联免疫吸附法检测血清食欲素A(Orexin A)(试剂盒货号: OXA-1001)、瘦素(Leptin)(试剂盒货号: LEP-1001)水平, 试剂盒由武汉吉利德生物、上海酶联生物科技等公司提供, 上述检测方法均按试剂盒说明书操作.
1.2.3 营养不良诊断: 根据GLIM标准[6], 于入院24 h内采用NRS2002[7]进行营养风险筛查, 对筛查阳性者进一步行营养不良诊断, 诊断需至少符合一项病因型指标和一项表现型指标. 病因型指标: (1)营养素吸收利用障碍或摄食减少: 吸收障碍致胃肠道症状, 或食物摄入不足50%正常需求量1 wk以上; 和(2)慢性疾病炎症或急性疾病损伤, 如癌症、充血性心力衰竭、慢阻肺及慢性肾病等, 本研究选取C反应蛋白(C-reactive protein, CRP)/白蛋白(albumin, ALB)比值, 参照孟洁等研究进行分层分析[8]. 表现型指标: (1)低身体质量指数(body mass index, BMI): BMI低于18.5 kg/m2; (2)非自主的体重减轻: 6 mo内体重下降超5%或至少6 mo体重下降超10%; 和(3)肌肉质量减少: 小腿围女性<33 cm, 男性<34 cm.
严格按纳排标准筛选研究对象, 调查开始前对参加调查者进行系统培训, 资料收集完毕后, 随机抽取10%进行核查, 确认无误后行双人录入并核对, 确保数据和结果的可靠真实.
(1)分析影响胃癌根治术后营养不良发生的因素; (2)分析胃癌根治术后营养不良的TAN模型; 和(3)分析营养不良对胃癌根治术后患者预后的影响.
统计学处理 采用SPSS 27.0行统计分析, 计数资料n(%)描述, χ2检验, 计量资料(mean±SD)描述, t检验. 采用逐步向前的Logistic回归分析胃癌根治术后营养不良发生的影响因素, BayesiaLab软件的树增益朴素贝叶斯算法建立TAN预测模型, 受试者工作特征曲线(receiver operating characteristic, ROC)分析其预测价值, 采用KaplanMeier曲线和Cox回归分析营养不良对预后的影响, 生存曲线间差异采用log-rank检验. P<0.05为差异有统计学意义.
两组年龄、手术切除范围、NRS2002评分、术后辅助化疗、术前营养不良、白蛋白、总蛋白、血红蛋白、血清Orexin A、血清Leptin比较, 差异均有统计学意义(P<0.05), 见表1. 将表1中除年龄外, P<0.05的因素纳入Logistic回归分析, 结果显示控制混杂因素(年龄), 全胃切除、NRS2002≥3分、术后辅助化疗、术前营养不良、血清Leptin是胃癌根治术后营养不良的危险因素, 白蛋白、血清Orexin A是其保护因素(P<0.05), 见表2.
| 项目 | 营养不良组(n = 169) | 非营养不良组(n = 77) | t/χ2值 | P值 |
| 性别 | 0.107 | 0.744 | ||
| 男 | 115(68.05) | 49(63.64) | ||
| 女 | 54(31.95) | 28(36.36) | ||
| 年龄(岁) | 71.20±10.57 | 68.12±8.39 | 2.253 | 0.025 |
| 白蛋白(g/L) | 32.68±3.47 | 37.54±3.20 | 10.483 | <0.001 |
| 总蛋白(g/L) | 58.96±6.40 | 63.71±7.18 | 5.193 | <0.001 |
| 血红蛋白(g/L) | 105.95±18.17 | 118.32±20.41 | 4.761 | <0.001 |
| 糖尿病史 | 0.081 | 0.776 | ||
| 有 | 24(14.20) | 12(15.58) | ||
| 无 | 145(85.80) | 65(84.42) | ||
| 高血压史 | 0.233 | 0.629 | ||
| 有 | 37(21.89) | 19(24.68) | ||
| 无 | 132(78.11) | 58(75.32) | ||
| 病理类型 | 0.512 | 0.489 | ||
| 管状腺癌 | 78(46.15) | 34(44.16) | ||
| 黏液腺癌 | 16(9.47) | 8(10.39) | ||
| 乳头状腺癌 | 29(17.16) | 15(19.48) | ||
| 低分化腺癌 | 46(27.22) | 20(25.97) | ||
| 临床分期 | 0.712 | 0.308 | ||
| Ⅰ期 | 65(38.46) | 28(36.36) | ||
| Ⅱ期 | 63(37.28) | 27(35.06) | ||
| Ⅲ期 | 41(24.26) | 22(28.57) | ||
| 手术切除范围 | 8.842 | 0.003 | ||
| 全胃 | 96(56.80) | 28(36.36) | ||
| 远端胃大部切除 | 73(43.20) | 49(63.64) | ||
| NRS2002评分(分) | 47.801 | <0.001 | ||
| <3 | 44(26.04) | 56(72.73) | ||
| ≥3 | 125(73.96) | 21(27.27) | ||
| 术后辅助化疗 | 10.706 | <0.001 | ||
| 有 | 138(81.66) | 48(62.34) | ||
| 无 | 31(18.34) | 29(37.66) | ||
| 术前营养不良 | 9.789 | 0.002 | ||
| 有 | 62(36.69) | 13(16.88) | ||
| 无 | 107(63.31) | 64(83.12) | ||
| 血清Orexin A(ng/mL) | 7.96±2.28 | 12.18±3.75 | 10.879 | <0.001 |
| 血清Leptin(ng/mL) | 8.16±2.09 | 5.29±1.43 | 10.934 | <0.001 |
| 影响因素 | 单因素 | 多因素 | ||
| OR(95%CI) | P值 | OR(95%CI) | P值 | |
| 手术切除范围(远端胃大部切除 = 0, 全胃 = 1) | 4.268(1.529-12.308) | <0.001 | 6.302(1.635-24.854) | <0.001 |
| NRS2002评分<3分 = 0, ≥3分 = 1 | 5.174(1.865-15.764) | <0.001 | 5.675(1.214-18.986) | <0.001 |
| 术后辅助化疗(无 = 0, 有 = 1) | 3.208(1.236-9.752) | <0.001 | 4.752(1.375-13.859) | <0.001 |
| 术前营养不良(无 = 0, 有 = 1) | 4.103(1.485-11.785) | <0.001 | 5.102(1.209-15.447) | <0.001 |
| 白蛋白(g/L) | 0.913(0.842-0.936) | <0.001 | 0.875(0.821-0.937) | <0.001 |
| 血清Orexin A(ng/mL) | 0.832(0.813-0.924) | <0.001 | 0.911(0.835-0.948) | <0.001 |
| 血清Leptin(ng/mL) | 1.056(1.018-1.175) | <0.001 | 1.023(1.025-1.096) | <0.001 |
| 总蛋白(g/L) | 1.532(0.985-2.326) | >0.05 | - | - |
| 血红蛋白(g/L) | 1.063(1.021-1.132) | <0.001 | 0.976(0.869-1.326) | >0.05 |
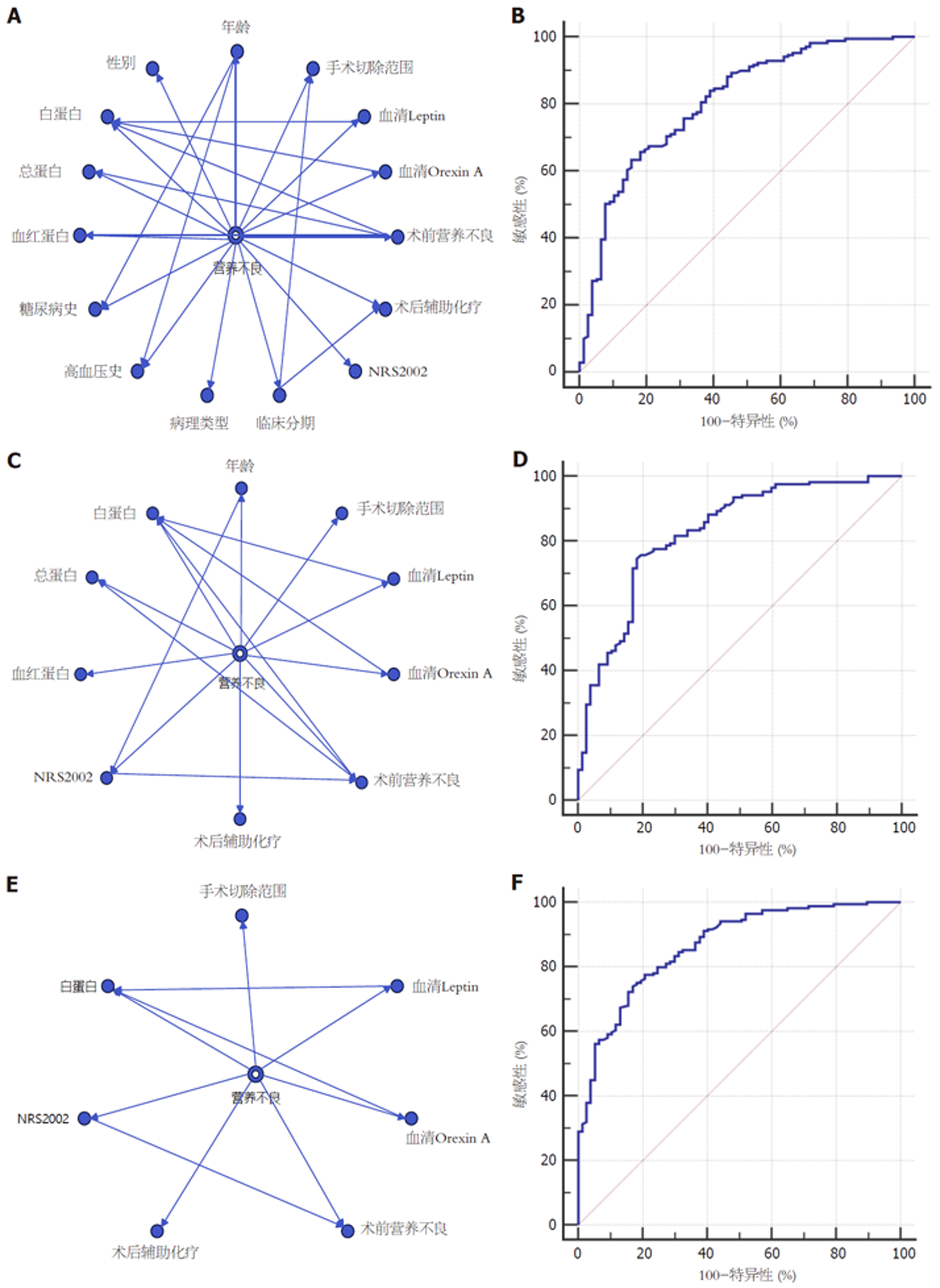
采用BayesiaLab软件的贝叶斯算法构建TAN模型, 首先将表1中15个临床病理学因素构建TAN模型, 该模型的曲线下面积(area under the curve, AUC)为0.807(95%CI: 0.752-0.854), 见图1A和B; 进一步将表1中P<0.05的10个因素构建TAN模型, 该模型的AUC为0.828(95%CI: 0.775-0.873), 见图1C和D; 最后根据Logistic回归分析结果, 纳入7个独立影响因素构建TAN模型, 该模型的AUC为0.866(95%CI: 0.817-0.906), 见图1E和F.
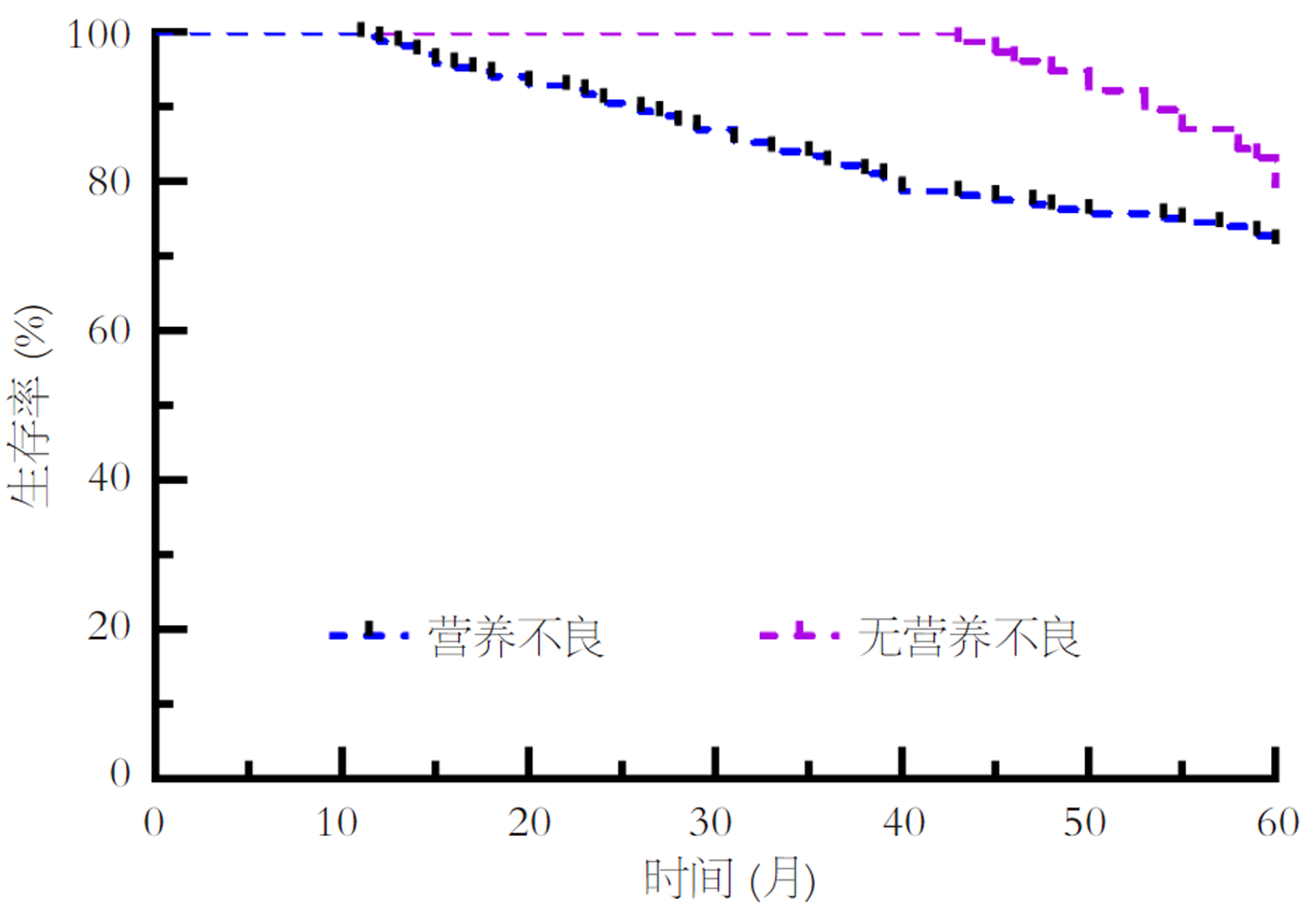
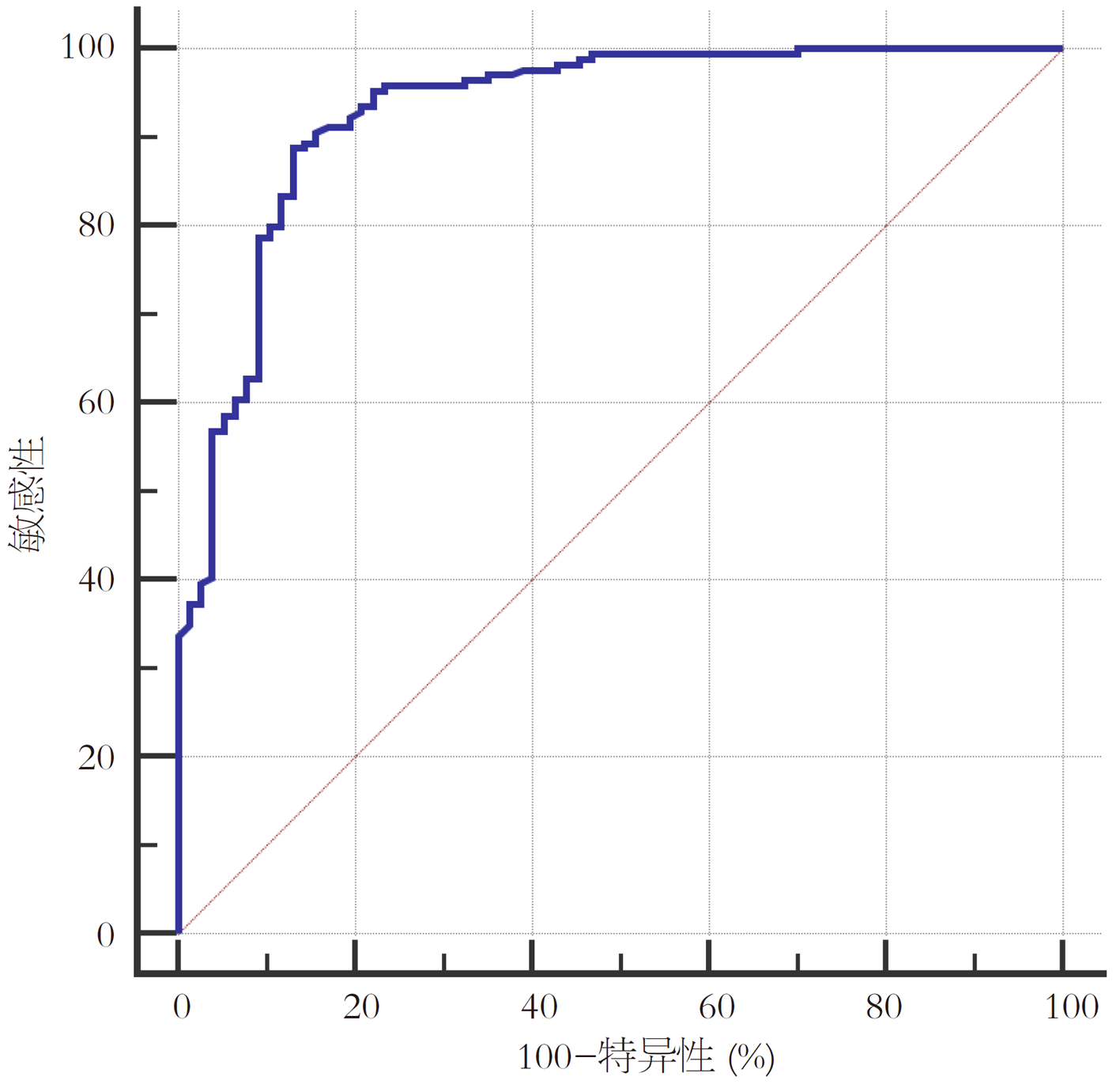
Kaplan Meier显示, 与营养不良患者相比, 术后营养正常患者预后更好(χ2 = 4.685, P<0.05), 见图2. 为进一步明确营养不良各核心组分对预后的独立影响, 本研究将GLIM标准中的关键指标纳入Cox回归分析, 包括3项表现型指标(非自主体重减轻、肌肉质量减少、低BMI)、2项病因型指标(营养素吸收利用障碍、CRP/ALB比值). Cox回归分析显示, 非自主体重减轻、低BMI、肌肉质量减少、CRP/ALB比值是影响胃癌根治术后预后的重要因素, 见表3. ROC评价基于GLIM标准的营养不良对胃癌根治术后患者预后的诊断效能, AUC为0.930(95%CI: 0.890-0.958), 敏感性、特异性分别为88.76%、87.01%, 见图3.
| GLIM标准 | HR(95%CI) | P值 |
| 非自重的体重减轻 | ||
| 正常 | 参考 | |
| 营养不良 | 10.652(1.652-42.895) | <0.001 |
| 营养素吸收利用障碍 | ||
| 正常 | 参考 | |
| 营养不良 | 2.315(1.015-3.652) | >0.05 |
| 肌肉质量减少 | ||
| 正常 | 参考 | |
| 营养不良 | 5.108(1.240-31.641) | <0.001 |
| 低BMI | ||
| 正常 | 参考 | |
| 营养不良 | 4.629(1.123-25.784) | <0.001 |
| CRP/ALB比值 | ||
| <0.09 | 参考 | |
| ≥0.09 | 9.657(1.185-37.265) | <0.001 |
营养是维持生命活动的物质基础, 研究报道[9], 胃癌术后患者的营养状态直接影响术后并发症、康复进程及长期生存质量. 本研究发现, 246例胃癌根治术后患者营养不良发生率为68.70%, 高于内镜术后早期胃癌患者的56.25%[10], 略低于胃癌化疗患者的 69.74%[11]. 这提示胃癌患者普遍存在较高的营养不良风险, 且其发生在不同群体间存在异质性, 因此对本地区胃癌根治术后患者的营养不良现况及其影响因素进行分析十分必要.
TAN是基于图论与概率论的数学模型, 由节点、带方向的有向边构成, 即变量与依赖, 通过条件概率以量化变量之间的关联性[12]. 该模型的核心作用是处理不确定性推理, 通过因果链表达变量之间的条件依赖关系, 以实现诊断、预测和决策优化[13,14]. 本研究首次将TAN模型应用于胃癌根治术后患者的营养不良预测, 结果发现, 基于Logistic结果构建的朴素TAN模型的AUC最大, 表现出较好的预测能力, 在胃癌根治术患者营养不良危险因素研究中具备较好运用前景. 此外, 经Logistic分析及TAN模型风险推理发现, 全胃切除、NRS2002≥3分、术前营养不良、术后辅助化疗、血清Leptin、白蛋白、血清Orexin A是胃癌根治术后营养不良的影响因素(P<0.05). 以往研究已证实[15,16], 胃癌术后营养不良与全胃切除、NRS2002≥3分、术前营养不良相关. 相比远端胃大部切除, 全胃切除范围更广, 造成肠道动力及分泌失衡、胃储备功能丧失, 增加营养不良风险. 因此, 在确保手术效果前提下, 应尽量保留残胃功能, 降低营养不良风险. NRS2002≥3分是营养风险筛查的临界值, 有效识别营养不良高危人群. 研究报道[17], 术前NRS2002≥3分者术后营养不良发生率高达47.0%. 因而建议将其作为核心评估工具以优化围术期营养管理路径. 此外, 2016版《胃癌胃切除手术加速康复外科专家共识》指出, 对于存在营养不良者, 术前需行≥1 wk的营养支持治疗, 以改善预后效果[18]. 术后辅助化疗在降低胃癌术后复发风险的同时, 可通过多重机制增加营养不良风险, 其对营养不良的预测价值与化疗方案密切相关. 研究报道[19], 化疗药物, 如奥沙利铂、卡培他滨的胃肠道毒性可直接引起呕吐、恶心及腹泻, 导致营养吸收障碍及摄入减少, 使术后体质量降低风险增加30%-40%. 此外, 化疗所诱导的慢性炎症可激活肌肉分解通路, 形成"化疗毒性-营养流失-免疫抑制"的恶性循环. 因此, 在选择化疗方案时需考虑营养风险, 对于高风险患者选择毒性较低的单药方案, 同步实施营养支持, 以降低营养相关不良事件概率. Leptin是脂肪细胞分泌的一种激素, 可通过下丘脑受体对食欲产生抑制, 而Orexin A可维持能量平衡并促进摄食[20]. 试验显示, 全胃切除后, 迷走神经及胃底细胞支配的缺失致使Orexin A、Leptin分泌紊乱, 引发食欲抑制和代谢亢进失衡, 临床表现为术后3-6 mo体质量大幅下降[21]. 研究报道[22], 术后Orexin A水平<30 pg/mL和Leptin>4.5 ng/mL的患者中, 严重营养不良在65%. 较白蛋白等传统指标, 其可提前8-12 wk预警营养恶化. 因此, 联合检测血清Orexin A、Leptin水平可为胃癌根治术后营养不良的早期预警和策略优化提供重要依据.
此外, 本研究发现, 基于GLIM诊断的营养不良是胃癌根治术后生存的独立危险因素, 其中GLIM标准的表现型指标是评估营养时必须考虑的关键表型特征. 研究报道[23,24], 体重减轻或低BMI的恶性肿瘤患者化疗毒副反应更为明显, 造成生活质量下降, 生存期缩短. 此外, GLIM标准指出可将白蛋白、CRP等评估炎症的实验室指标作为病因型指标, 但具体指标选取尚无定论. CRP/ALB比值是反映营养失衡和机体炎症的复合指标, 文献报道[25], 术前CRP/ALB比值升高与淋巴结转移、肿瘤浸润深度显著相关, 术后5年总生存率下降30%-35%. 本研究显示, 纳入CRP/ALB比值的GLIM诊断标准预测胃癌根治术后生存预后的AUC为0.930, 敏感性、特异性分别为88.76%、87.01%, 可进一步提升基于GLIM诊断的营养不良对胃癌根治术后生存情况的预测价值.
综上可知, 全胃切除、NRS2002≥3分、术后辅助化疗、术前营养不良、白蛋白、血清Orexin A、血清Leptin是胃癌根治术后营养不良的影响因素, 而基于GLIM诊断标准的营养不良对生存预后有重要影响, 且TAN构建的预测模型能反映胃癌根治术后营养不良的风险. 本研究存在以下局限性: 首先, 数据来源以回顾性单中心为主, 存在潜在选择偏倚及混杂因素干扰; 其次, 变量选择局限于常规指标, 缺乏其他多维度数据; 模型未充分整合分子相关生物学证据, 因果推断受限. 未来应开展前瞻性多中心研究, 纳入多维数据, 并探索机器学习和TAN混合建模方式以提升模型的可解释性与预测效能.
现有研究明确消化道重建方式、术前营养状态等与术后营养不良相关, 但多采用Logistic回归等传统统计方法构建预测模型, 难以解析多因素复杂交互效应. 此外, 营养不良倡议(global leadership initiative on malnutrition, GLIM)标准要求营养不良诊断需满足至少一个病因和一种表现型标准, 其与胃癌及其他肿瘤患者预后的关联性仍需进一步探究证实.
贝叶斯网络(tree augmented naive Bayes, TAN)因其在处理多变量、不确定性非线性关系和可视化因果推理方面的诸多优势, 逐渐被用于医疗领域的数据分析. 然而, TAN模型在胃癌术后营养状况研究中的应用仍鲜有报道.
基于TAN模型分析胃癌根治术后患者营养不良的相关因素及其对预后的影响.
选取2024-03/2025-01杭州市余杭区第二人民医院246例胃癌患者, 依GLIM标准诊断营养不良, 采用Logistics回归、TAN模型分析其影响因素及交互关系, 通过Kaplan-Meier、Cox回归分析营养不良对预后的影响, 并以受试者工作特征曲线评价其对术后生存率的预测价值.
Logistic回归显示, 全胃切除、NRS2002≥3分等为胃癌根治术后营养不良危险因素, 白蛋白、Orexin A为保护因素(P<0.05). TAN模型曲线下面积(area under the curve, AUC)最高0.866; 营养正常者预后更佳, GLIM标准预测预后AUC达0.930, 具有良好价值.
全胃切除、NRS2002≥3分、术后辅助化疗、术前营养不良、白蛋白、血清Orexin A、血清Leptin是胃癌根治术后营养不良的影响因素, 而基于GLIM诊断标准的营养不良对生存预后有重要影响, 且TAN构建的预测模型能反映胃癌根治术后营养不良的风险.
本研究显示, 纳入C反应蛋白/白蛋白比值的GLIM诊断标准预测胃癌根治术后生存预后的AUC为0.930, 敏感性、特异性分别为88.76%、87.01%, 可进一步提升基于GLIM诊断的营养不良对胃癌根治术后生存情况的预测价值.
| 1. | Kang MK, Lee HJ. Impact of malnutrition and nutritional support after gastrectomy in patients with gastric cancer. Ann Gastroenterol Surg. 2024;8:534-552. [PubMed] [DOI] |
| 2. | Wang HM, Wang TJ, Huang CS, Liang SY, Yu CH, Lin TR, Wu KF. Nutritional Status and Related Factors in Patients with Gastric Cancer after Gastrectomy: A Cross-Sectional Study. Nutrients. 2022;14:2634. [PubMed] [DOI] |
| 3. | Triantafillidis JK, Papakontantinou J, Antonakis P, Konstadoulakis MM, Papalois AE. Enteral Nutrition in Operated-On Gastric Cancer Patients: An Update. Nutrients. 2024;16:1639. [PubMed] [DOI] |
| 4. | 闫 慈, 古丽努尔· 阿卜杜热合曼, 张 旭, 孙 刚. 基于LASSO变量选择联合贝叶斯网络构建乳腺癌患者5年预后风险模型的建立与预测. 重庆医学. 2024;53:405-410, 417. [DOI] |
| 5. | 宋 明康, 徐 天朝, 贾 竑晓, 李 冬冬, 郑 思思, 尹 冬青, 李 雪. 基于聚类分析与贝叶斯网络的惊恐障碍中医证候规律探索. 首都医科大学学报. 2023;44:583-589. [DOI] |
| 6. | Fu L, Lei C, Chen Y, Xu X, Wu B, Dong L, Ye X, Zheng L, Gong D. Association of the rs3917647 polymorphism of the SELP gene with malnutrition in gastric cancer. Support Care Cancer. 2023;31:708. [PubMed] [DOI] |
| 7. | Wang J, Liu B, Chen J. Validity of the Global Leadership Initiative on Malnutrition criteria in East Asian patients with gastric cancer: a comprehensive narrative review. Front Nutr. 2024;11:1462487. [PubMed] [DOI] |
| 8. | 孟 洁, 康 亚丽, 任 更朴, 张 丽媛, 于 艳艳. 术前外周血纤维蛋白原与前白蛋白比值、C反应蛋白与前白蛋白比值、C反应蛋白与白蛋白比值与胃癌患者预后关系研究. 陕西医学杂志. 2024;53:987-990. [DOI] |
| 12. | Chen R, Luo L, Zhang YZ, Liu Z, Liu AL, Zhang YW. Bayesian network-based survival prediction model for patients having undergone post-transjugular intrahepatic portosystemic shunt for portal hypertension. World J Gastroenterol. 2024;30:1859-1870. [PubMed] [DOI] |
| 13. | Ma L, Cai B, Qiao ML, Fan ZX, Fang LB, Wang CB, Liu GZ. Risk factors assessment and a Bayesian network model for predicting ischemic stroke in patients with cardiac myxoma. Front Cardiovasc Med. 2023;10:1128022. [PubMed] [DOI] |
| 14. | Teng L, Zhang Y, Fang J, Liu X, Shi T, Qu C, Li J, Shen C. A Bayesian network meta-analysis for acute thrombosis after lower extremity artery endovascular treatment. Catheter Cardiovasc Interv. 2023;102:731-742. [PubMed] [DOI] |
| 16. | 王 家成, 孙 琳, 张 献娜, 宗 璐, 顾 凯利, 王 娟, 胡 磊, 任 春霞. GLIM标准下胃肠道恶性肿瘤手术患者营养状况调查及发生营养不良的影响因素分析. 现代肿瘤医学. 2023;31:3216-3221. [DOI] |
| 17. | Finze A, Vijgen GH, Betzler J, Orth V, Hetjens S, Reissfelder C, Otto M, Blank S. Malnutrition and vitamin deficiencies after surgery for esophageal and gastric cancer: A metanalysis. Clin Nutr ESPEN. 2024;60:348-355. [PubMed] [DOI] |
| 19. | Salas S, Cottet V, Dossus L, Fassier P, Ginhac J, Latino-Martel P, Romieu I, Schneider S, Srour B, Touillaud M, Touvier M, Ancellin R. Nutritional Factors during and after Cancer: Impacts on Survival and Quality of Life. Nutrients. 2022;14:2958. [PubMed] [DOI] |
| 21. | Jagric T, Hladnik G, Kolaric R, Dugonik M, Homsak E. Does leptin cause proximal gastric cancer in the obese? The role of serum leptin in the etiology of proximal gastric cancer. Horm Mol Biol Clin Investig. 2023;44:393-400. [PubMed] [DOI] |
| 22. | Krishnan M P S, Gupta A, Gupta S, Rani S, Mirza AA, Goyal B. Association of Serum Leptin With Body Mass Index in Gallbladder Cancer Patients: A Pilot Study. Cureus. 2023;15:e39018. [PubMed] [DOI] |
| 23. | 游 利江, 葛 杰, 刘 婷, 赵 庭雨, 谢 凯强, 刘 合利, 唐 密密. NRS 2002和PG-SGA在胃肠道恶性肿瘤患者中的应用. 胃肠病学. 2023;28:432-436. [DOI] |
| 24. | 孙 祺, 刘 畅, 叶 健乔, 黄 文博, 徐 宇航, 姚 程智, 赵 伟. 局部进展期中低位直肠癌单纯新辅助化疗与新辅助放化疗的疗效比较. 西安交通大学学报(医学版). 2024;45:278-283. [DOI] |
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): 0
D级 (一般): D
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁