修回日期: 2026-03-20
接受日期: 2026-03-23
在线出版日期: 2026-03-28
尽管早期胃癌患者内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)术后复发的相关研究已逐步开展, 但仍存在一些挑战, 尤其是如何有效预测术后复发的高危因素, 以便在临床中采取针对性防控措施, 从而降低复发率.
本研究旨在探讨幽门螺杆菌(Helicobacter pylori, H. pylori)感染早期胃癌患者内镜黏膜下剥离术ESD后复发的危险因素, 并构建预测模型.
回顾性分析2020-01/2022-01在杭州市余杭区第二人民医院接受ESD治疗的152例. H. pylori感染早期胃癌患者的临床资料, 根据术后3年随访结果, 患者分为复发组(38例)和未复发组(114例). 通过Lasso回归分析和10折交叉验证, 筛选出与术后复发相关的潜在预测因子, 并根据这些因子构建复发预测模型. 使用受试者工作特征曲线(receiver operating characteristic, ROC)、校准曲线和决策曲线验证模型的预测效能.
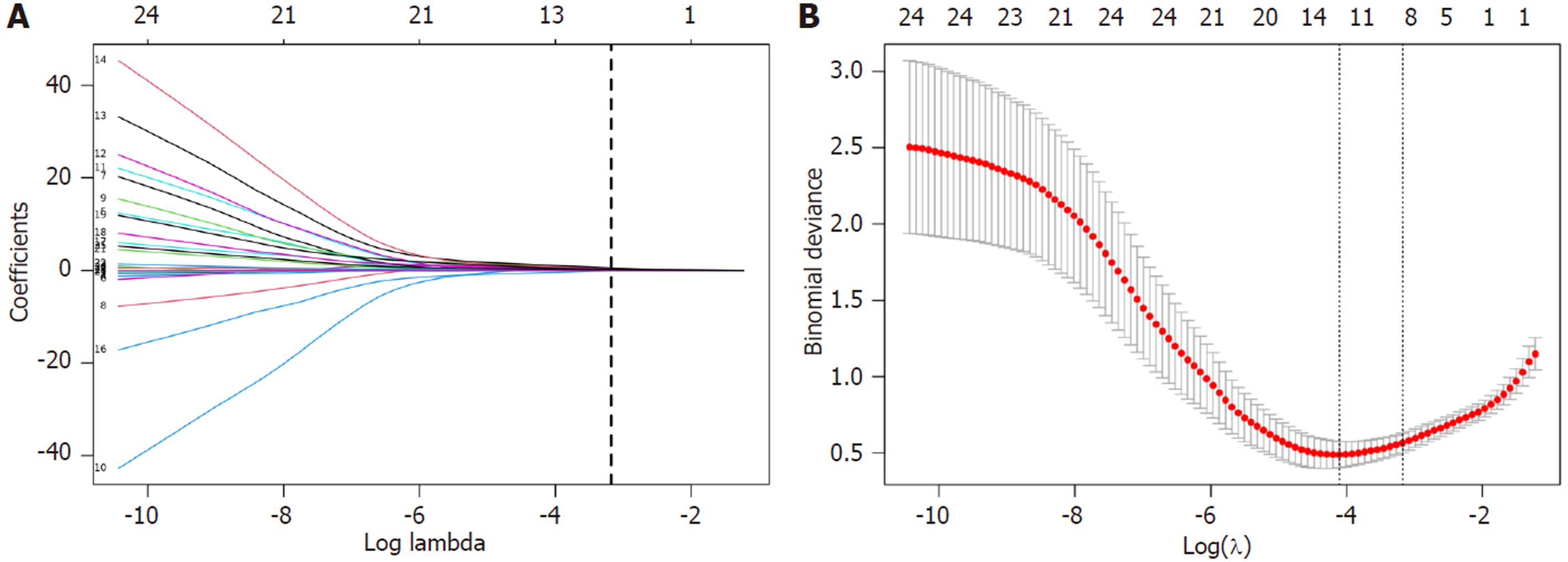
通过Lasso回归分析, 选取最小二乘法一个标准差(λ = 0.0417)对应的模型, 最终筛选出9个与H. pylori感染早期胃癌患者ESD术后复发相关的潜在预测因子, 包括家族肿瘤史、肿瘤直径、分化程度、浸润深度、Ki-67阳性、H. pylori转阴失败、糖类抗原724(carbohydrate antigen 724, CA724)、胰蛋白酶原Ⅰ(pepsinogen Ⅰ, PGⅠ)、胃泌素17(gastrin-17, G-17). 复发组与未复发组在这些因子上的差异具有统计学意义(P<0.05). 通过构建的列线图预测模型, ROC曲线下面积为0.975, 模型的预测值与实际值一致性较高, 具有良好的临床应用价值.
家族肿瘤史、肿瘤直径、分化程度、浸润深度、Ki-67阳性、H. pylori转阴失败、CA724、PGⅠ、G-17为H. pylori感染早期胃癌患者ESD术后复发的独立危险因素. 基于这些因素构建的列线图预测模型, 具有良好的临床预测价值, 可辅助识别高风险患者并指导临床干预, 降低复发率并改善预后.
核心提要: 本研究旨在分析幽门螺杆菌感染早期胃癌患者内镜黏膜下剥离术术后复发的影响因素, 并基于这些因素构建一个列线图预测模型. 通过整合临床数据和Lasso回归分析, 我们期望为临床提供一个有效的术后复发预测工具, 帮助早期识别高风险患者, 指导临床防治策略的制定.
引文著录: 姚智刚, 摇顺华, 鲁雅儿. 幽门螺杆菌感染早期胃癌ESD术后复发风险预测模型的构建. 世界华人消化杂志 2026; 34(3): 265-274
Revised: March 20, 2026
Accepted: March 23, 2026
Published online: March 28, 2026
Although studies on postoperative recurrence after endoscopic submucosal dissection (ESD) in patients with early gastric cancer have gradually increased, several challenges remain. In particular, a key challenge lies in how to effectively identify high-risk factors for postoperative recurrence so as to implement targeted prevention and control measures in clinical practice and thereby reduce the recurrence rate.
To analyze the risk factors for postoperative recurrence in early gastric cancer patients with Helicobacter pylori (H. pylori) infection after ESD, and to construct a nomogram-based risk prediction model for recurrence.
This study included 152 H. pylori-infected early gastric cancer patients who underwent ESD at Second People's Hospital of Yuhang District from January 2020 to December 2022. Based on a 3-year follow-up after surgery, the patients were divided into a recurrence group (38 cases) and a non-recurrence group (114 cases). Lasso regression analysis and 10-fold cross-validation were used to identify potential predictors associated with postoperative recurrence, and a recurrence prediction model was constructed based on these factors. The model's predictive performance was evaluated using receiver operating characteristic (ROC) curves, calibration curves, and decision curves.
Lasso regression analysis with a penalty coefficient of λ = 0.0417 identified 9 potential predictors associated with non-cardiac gastric cancer, including family cancer history, tumor diameter, differentiation degree, invasion depth, Ki-67 positive expression, H. pylori eradication failure, carbohydrate antigen 724 (CA724), pepsinogen I (PGI), and gastrin-17 (G-17). Significant differences were observed between the recurrence and non-recurrence groups in these factors (P < 0.05). The nomogram-based prediction model constructed based on these factors showed a high consistency between predicted and actual values, with an area under the ROC curve of 0.975, demonstrating its strong clinical utility.
Family cancer history, tumor diameter, differentiation degree, invasion depth, Ki-67 positive expression, H. pylori eradication failure, CA724, PGI, and G-17 are independent risk factors for postoperative recurrence in H. pylori-infected early gastric cancer patients after ESD. The nomogram prediction model constructed based on these factors has excellent clinical predictive value and can assist in identifying high-risk patients, guiding clinical interventions, and reducing recurrence rates, ultimately improving prognosis.
- Citation: Yao ZG, Yao SH, Lu YE. Construction of a risk prediction model for recurrence of early gastric cancer after endoscopic submucosal dissection in patients with Helicobacter pylori infection. Shijie Huaren Xiaohua Zazhi 2026; 34(3): 265-274
- URL: https://www.wjgnet.com/1009-3079/full/v34/i3/265.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v34.i3.265
核心提要: 本研究旨在分析幽门螺杆菌感染早期胃癌患者内镜黏膜下剥离术术后复发的影响因素, 并基于这些因素构建一个列线图预测模型. 通过整合临床数据和Lasso回归分析, 我们期望为临床提供一个有效的术后复发预测工具, 帮助早期识别高风险患者, 指导临床防治策略的制定.
2020年, 胃癌位列全球第五大常见的恶性肿瘤, 全球新增病例约为110万例, 且是导致癌症死亡的第四大原因, 造成约80万人死亡[1]. 在全球范围内, 超过85%的胃癌病例发生在那些人类发展指数较高或极高的国家, 其中分别有59万例和36万例[1]. 亚洲, 特别是中国, 是胃癌病例最多的地区, 新增病例接近82万, 死亡人数约58万[2]. 据估计, 胃癌的五年生存率不足20%[3]. 对于早期胃癌且未发现转移的患者, 内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)已成为首选治疗方法之一[4]. 多数患者术后可以实现治愈, 但也有部分患者出现ESD术后复发[5]. 幽门螺杆菌(Helicobacter pylori, H. pylori)感染已被证明是胃癌发生和发展的重要因素, H. pylori感染通过分泌空泡毒素等, 增加胃酸分泌, 损伤胃黏膜屏障并引起炎症反应, 进一步提高胃黏膜病变风险并增加ESD术后复发的可能性[6,7].
尽管ESD术后复发的相关研究已逐步开展, 但仍存在一些挑战, 尤其是如何有效预测术后复发的高危因素, 以便在临床中采取针对性防控措施, 从而降低复发率. 近年来, 研究指出[8,9]体质量指数(body mass index, BMI)、年龄及胃泌素17(gastrin-17, G-17)的异常表达等因素与早期胃癌患者ESD术后复发独立相关. 然而, 目前关于早期胃癌患者ESD术后复发的风险预测研究较为有限, 大多数研究侧重于影响因素分析, 缺少相关预测模型的构建.
因此, 本研究旨在分析H. pylori感染早期胃癌患者ESD术后复发的影响因素, 并基于这些因素构建一个列线图预测模型. 通过整合临床数据和Lasso回归分析, 我们期望为临床提供一个有效的术后复发预测工具, 帮助早期识别高风险患者, 指导临床防治策略的制定.
1.1 材料 本研究为单中心回顾性研究, 选取2020-01/2022-01在杭州市余杭区第二人民医院, 接受ESD治疗的H. pylori感染早期胃癌患者152例. 根据术后3年随访结果, 患者分为复发组(38例)和未复发组(114例). 纳入标准包括: (1)经临床病理确诊为早期胃癌[10], 并接受ESD治疗; (2)术前经13C尿素呼气试验、快速尿素酶试验或病理检查证实存在H. pylori感染; (3)首次确诊, 未接受任何抗肿瘤治疗; (4)病灶局限于胃黏膜层或黏膜下层; 和(5)患者知情同意参与研究. 排除标准包括: (1)伴有精神或心理疾病, 无法配合治疗; (2)语言交流障碍; (3)合并其他恶性肿瘤; (4)合并严重感染性疾病以及未检测到H. pylori感染或H. pylori感染状态不明确者; (5)存在免疫或循环系统疾病; (6)重要脏器功能不全; 和(7)伴有淋巴结转移或远处转移. 脱落标准包括: (1)突发重大疾病、随访期间失联或意外死亡; 和(2)患者自行退出研究.
本研究经医院伦理委员会批准, 符合《赫尔辛基宣言》原则. 研究为回顾性分析, 患者信息均已匿名处理, 免除知情同意.
1.2.1 资料收集: 通过在知网、万方、PubMed等在线数据库中检索, 以"HP感染"、"早期胃癌"、"ESD"、"复发"、"风险因素"等为关键词, 查阅相关文献, 并结合患者病情确定潜在的影响因素. 研究小组由两名成员组成, 负责信息的采集工作. 主要通过病历回顾和辅助检查结果追踪, 收集以下患者临床信息: 性别、年龄、BMI、吸烟史、饮酒史、高血压、糖尿病、高脂血症、家族肿瘤史、组织类型(腺癌、其他)、肿瘤部位(胃体、胃窦、贲门胃底)、肿瘤直径(<2 cm、≥2 cm)、内镜分型(凹陷型、平坦型、隆起型)、分化程度(中低分化、高分化)、病灶数目(多发、单发)、浸润深度(黏膜层、黏膜下层)、T分期(T1a、T1b)、Ki-67阳性(<50%、≥50%)、H. pylori转阴失败、R0切除、手术时间、血清糖类抗原125(carbohydrate antigen 125, CA125)、癌胚抗原(carcinoembryonic antigen, CEA)、癌抗原19-9(carbohydrate antigen 19-9, CA19-9)等.
1.2.2 随访: 所有患者自ESD术后第1天开始进行随访, 主要通过门诊复查形式, 随访期为3年. 第1年每3 mo复查一次, 之后每6 mo复查一次. 随访的终点事件为胃癌复发或随访截止时间的到达.
1.2.3 复发评估标准: 术后复发的判定结合胃镜表现与病理学结果综合确定[10]. 所有患者按照既定随访方案定期接受胃镜复查, 必要时行窄带成像放大内镜检查. 对复查中发现的可疑病变, 如ESD瘢痕处黏膜不规则隆起、局部充血糜烂、边界不清的新生病灶、表面微血管或微表面结构异常等, 均行靶向活检并送病理检查.
本研究将复发定义为ESD术后随访期间经胃镜提示可疑病变, 并经病理证实为高级别上皮内瘤变或腺癌者. 根据病灶发生部位不同, 将复发分为原位复发和异时复发: 原位复发指病变发生于原ESD切除瘢痕处或其邻近区域; 异时复发指病变发生于胃内其他非原切除部位. 若患者同时满足上述任一情况, 均判定为复发, 并纳入复发组.
H. pylori转阴失败的判定依据根除治疗后的复查结果. 所有患者在ESD术后接受标准幽门螺杆菌根除治疗, 并于停药4 wk后采用13C尿素呼气试验进行检测, 检测前停用质子泵抑制剂至少2 wk. 若检测结果仍为阳性, 则判定为H. pylori转阴失败; 若为阴性, 则判定为H. pylori成功根除. 对于未按规定时间复查或结果不明确者, 不纳入相关变量分析.
对病理结果不明确者, 由2名具有副高级及以上职称的病理医师独立复核; 若结果存在分歧, 则经讨论后形成一致意见. 对仅有胃镜可疑表现但病理未证实复发者, 不判定为复发.
1.2.4 质量控制: (1)信息采集小组成员需经过统一的培训和考核, 确保数据的准确性; (2)数据录入与核对由两名研究人员独立完成, 以保证数据的可靠性和一致性; 和(3)所有检查结果的判读由具有5年以上临床经验的医师进行, 并采用双盲形式, 若有争议, 需进行协商并达成一致结果.
本研究的观察指标包括: (1)比较复发组与未复发组的临床资料, 重点分析两组在性别、年龄、BMI、吸烟史、饮酒史、高血压、糖尿病、高脂血症、家族肿瘤史等人口学特征, 以及肿瘤直径、分化程度、病灶数目、浸润深度、Ki-67表达、H. pylori转阴失败等肿瘤特征上的差异, 以识别可能与术后复发相关的临床因素; (2)通过单因素和多因素分析, 进一步筛选出与ESD术后复发独立相关的因素, 特别是患者的肿瘤特征和生物标志物, 如肿瘤直径、分化程度、Ki-67、CA724、中性粒细胞与淋巴细胞比值(neutrophil-to-lymphocyte ratio, NLR)、G-17等, 以分析其对复发的影响; 和(3)基于患者一般资料、肿瘤病理特征及实验室指标, 先进行组间比较和变量筛选, 再采用Lasso回归进行降维, 并将筛选出的候选变量纳入多因素Logistic回归分析, 最终确定独立危险因素并构建列线图预测模型. 并通过受试者工作特征曲线(receiver operating characteristic, ROC)曲线、校准曲线等内部验证方法评估该模型的预测性能和准确性, 以期为临床提供有效的复发预测工具.
统计学处理 数据分析采用SPSS 27.0统计学软件进行. 计数资料以n(%)表示, 采用卡方检验(χ2); 计量资料若近似正态分布, 则以均值±标准差(mean±SD)表示, 采用t检验; Lasso-Logistic回归分析用于筛选影响因素; 列线图预测模型的构建过程中, 使用ROC、校准曲线、决策曲线来评估模型的预测效能. 此外, 还绘制了列线图预测模型预测术后复发的临床影响曲线, 进一步验证该模型在临床中的应用价值. 统计学显著性设定为P<0.05, 检验水准为α = 0.05. 变量筛选遵循"单因素分析初筛+Lasso回归降维+多因素Logistic回归确定独立危险因素"的原则. 最终列线图模型仅纳入多因素Logistic回归分析中具有统计学意义的独立危险因素.
本研究共纳入152例接受ESD治疗的H. pylori感染早期胃癌患者, 所有患者均完成随访, 其中38例患者发生复发, 纳入复发组, 114例患者未复发, 纳入未复发组. 两组患者在性别、年龄、BMI、高血压、糖尿病、高脂血症、胃息肉史、肿瘤部位、T分期、手术时间及术前血清CA125、CEA、CA19-9水平等方面比较, 差异均无统计学意义(P>0.05); 而在吸烟史、饮酒史、家族肿瘤史、肿瘤直径、分化程度、病灶数目、浸润深度、Ki-67阳性表达、H. pylori转阴失败、术前血清CA724、胰蛋白酶原Ⅰ(pepsinogen Ⅰ, PGⅠ)及G-17水平等方面比较, 差异均有统计学意义(P<0.05). 上述结果提示, 吸烟史、饮酒史、家族肿瘤史、肿瘤直径、分化程度、病灶数目、浸润深度、Ki-67阳性表达、H. pylori转阴失败及部分血清学指标可能与H. pylori感染早期胃癌患者ESD术后复发相关, 可作为后续Lasso回归和多因素Logistic回归分析的候选变量. 具体见表1.
| 项目 | 复发组(n = 38) | 未复发组(n = 114) | t/χ2 | P值 |
| 性别 | 0.928 | 0.335 | ||
| 男 | 21(55.26) | 70(61.40) | ||
| 女 | 16(42.11) | 44(38.40) | ||
| 年龄(岁) | 59.36±8.14 | 58.51±9.21 | 0.507 | 0.613 |
| 医保 | ||||
| 有 | 10(26.32) | 29(25.44) | ||
| 无 | 28(73.68) | 85(74.56) | ||
| BMI(kg/m2) | 23.09±1.82 | 22.84±1.77 | -0.891 | 0.374 |
| 吸烟史 | 10.976 | 0.001 | ||
| 有 | 25(65.79) | 40(35.09) | ||
| 无 | 13(34.21) | 74(64.91) | ||
| 饮酒史 | 8.941 | 0.003 | ||
| 有 | 20(52.63) | 30(26.32) | ||
| 无 | 18(47.37) | 84(73.68) | ||
| 高血压 | 12(35.29) | 31(27.19) | 0.270 | 0.603 |
| 糖尿病 | 10(26.32) | 24(21.05) | 0.455 | 0.500 |
| 高脂血症 | 6(15.793) | 15(13.16) | 0.166 | 0.684 |
| 家族肿瘤史 | 13.521 | <0.001 | ||
| 有 | 18(47.37) | 20(17.54) | ||
| 无 | 20(52.63) | 94(82.46) | ||
| 胃息肉史 | 0.142 | 0.706 | ||
| 有 | 3(7.89) | 7(6.14) | ||
| 无 | 35(92.11) | 107(93.86) | ||
| 肿瘤部位 | 0.338 | 0.845 | ||
| 胃体 | 17(44.74) | 54(47.37) | ||
| 胃窦 | 12(31.58) | 38(33.33) | ||
| 贲门胃底 | 9(23.68) | 22(19.30) | ||
| 肿瘤直径 | 8.992 | 0.003 | ||
| ≥2 cm | 22(57.89) | 35(30.70) | ||
| <2 cm | 16(42.11) | 79(69.30) | ||
| 分化程度 | 7.639 | 0.006 | ||
| 中低分化 | 20(52.63) | 32(28.07) | ||
| 高分化 | 18(47.37) | 82(71.93) | ||
| 病灶数目 | 4.943 | 0.026 | ||
| 多发 | 6(15.79) | 5(4.67) | ||
| 单发 | 32(84.21) | 102(95.33) | ||
| 浸润深度 | 6.896 | 0.009 | ||
| 黏膜层 | 13(34.21) | 67(58.77) | ||
| 黏膜下层 | 25(65.79) | 47(41.23) | ||
| T分期 | 0.650 | 0.420 | ||
| T1a | 24(63.16) | 80(70.18) | ||
| T1b | 14(36.84) | 34(29.82) | ||
| Ki-67阳性 | 13.360 | <0.001 | ||
| ≥50% | 28(73.68) | 45(39.47) | ||
| <50% | 10(26.32) | 69(60.53) | ||
| H. pylori转阴失败 | 14(36.84) | 20(17.54) | 6.112 | 0.013 |
| CA125(kU/mL) | 59.08±9.38 | 57.09±8.22 | 1.247 | 0.214 |
| CEA(μg/L) | 14.79±2.25 | 14.16±3.22 | 1.117 | 0.266 |
| CA724(U/mL) | 19.52±4.09 | 16.88±2.69 | 4.554 | <0.001 |
| PGⅠ(ng/mL) | 77.61±21.73 | 97.84±21.51 | 3.777 | <0.001 |
| PGⅡ(ng/mL) | 19.50(9.35-38.88) | 18.62(13.59-20.74) | Z = 0.62 | 0.535 |
| G-17(μg/L) | 27.64±7.22 | 15.42±5.17 | 11.357 | <0.001 |
将术后是否复发作为因变量, 将单因素分析中差异有统计学意义及临床上具有潜在意义的变量纳入Lasso回归分析, 结合10折交叉验证筛选候选预测因子. 在λ = 0.0417时获得较优模型, 共筛选出9个候选变量, 包括家族肿瘤史、肿瘤直径、分化程度、浸润深度、Ki-67阳性、H. pylori转阴失败、CA724、PGⅠ和G-17. 上述变量进一步纳入多因素Logistic回归分析(图1).
将Lasso筛选出的9个候选变量纳入多因素Logistic回归模型, 进一步分析其与ESD术后复发的独立相关性. 结果显示, 家族肿瘤史、肿瘤直径、分化程度、CA724及G-17为H. pylori感染早期胃癌患者ESD术后复发的独立危险因素(P<0.05); 浸润深度、Ki-67阳性、H. pylori转阴失败及PGⅠ未达到统计学差异(P>0.05). 具体见表2.
| 变量 | B | 标准误差 | 瓦尔德 | 显著性 | OR | OR的95%CI | |
| 下限 | 上限 | ||||||
| 家族肿瘤史(1) | 2.61 | 1.104 | 5.585 | 0.018 | 13.595 | 1.561 | 118.404 |
| 肿瘤直径(1) | 2.721 | 1.141 | 5.687 | 0.017 | 15.19 | 1.624 | 142.123 |
| 分化程度(1) | 2.364 | 1.023 | 5.337 | 0.021 | 10.637 | 1.431 | 79.062 |
| 浸润深度(1) | -1.994 | 1.096 | 3.309 | 0.069 | 0.136 | 0.016 | 1.167 |
| Ki-67阳性(1) | 1.458 | 1.087 | 1.797 | 0.18 | 4.296 | 0.51 | 36.189 |
| H. pylori转阴失败(1) | 1.628 | 1.096 | 2.209 | 0.137 | 5.096 | 0.595 | 43.643 |
| CA724 | 0.342 | 0.146 | 5.485 | 0.019 | 1.408 | 1.057 | 1.874 |
| PGⅠ | -0.04 | 0.022 | 3.204 | 0.073 | 0.961 | 0.92 | 1.004 |
| G-17 | 0.55 | 0.154 | 12.813 | 0.000 | 1.733 | 1.282 | 2.342 |
| 常量 | -19.079 | 5.941 | 10.312 | 0.001 | 0 | ||
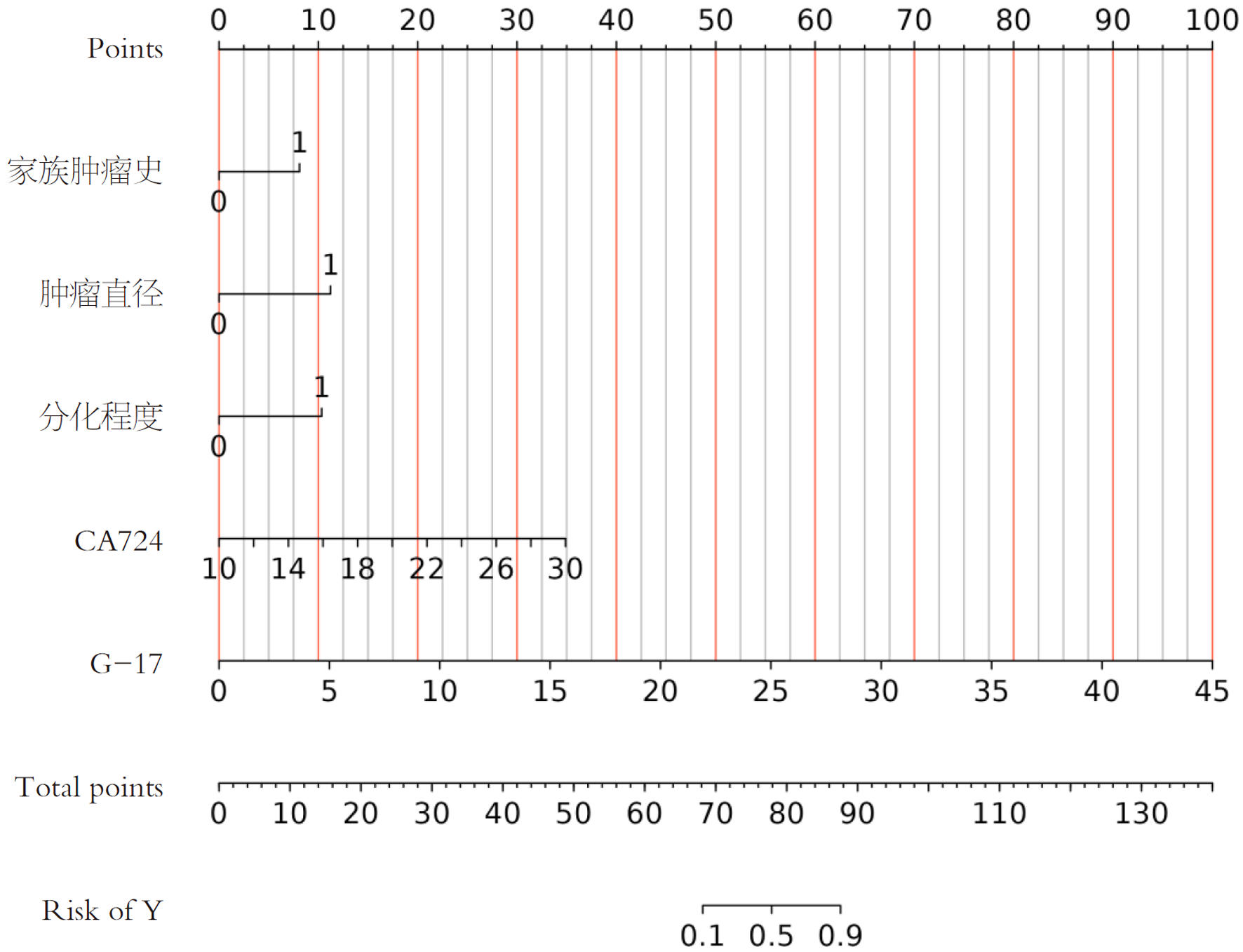
经Lasso回归筛选获得候选变量, 进一步纳入多因素Logistic回归分析后, 最终有5个变量具有统计学意义(P<0.05), 并用于构建列线图预测模型. 以H. pylori感染早期胃癌患者ESD术后复发为结局变量, 将多因素Logistic回归分析筛选出的独立危险因素, 即家族肿瘤史、肿瘤直径、分化程度、CA724和G-17, 纳入列线图预测模型构建. 根据各变量回归系数赋予相应权重, 建立术后复发风险列线图模型(图2).
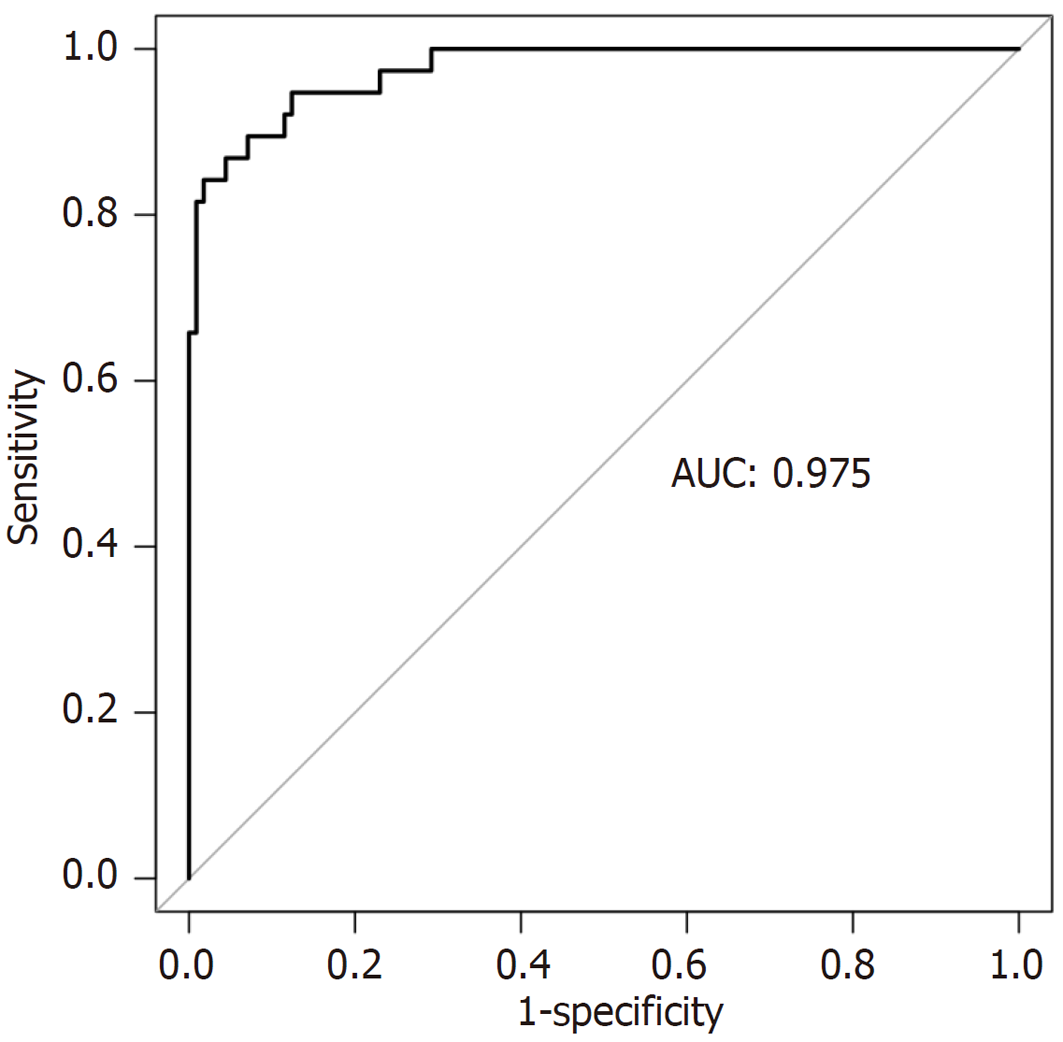
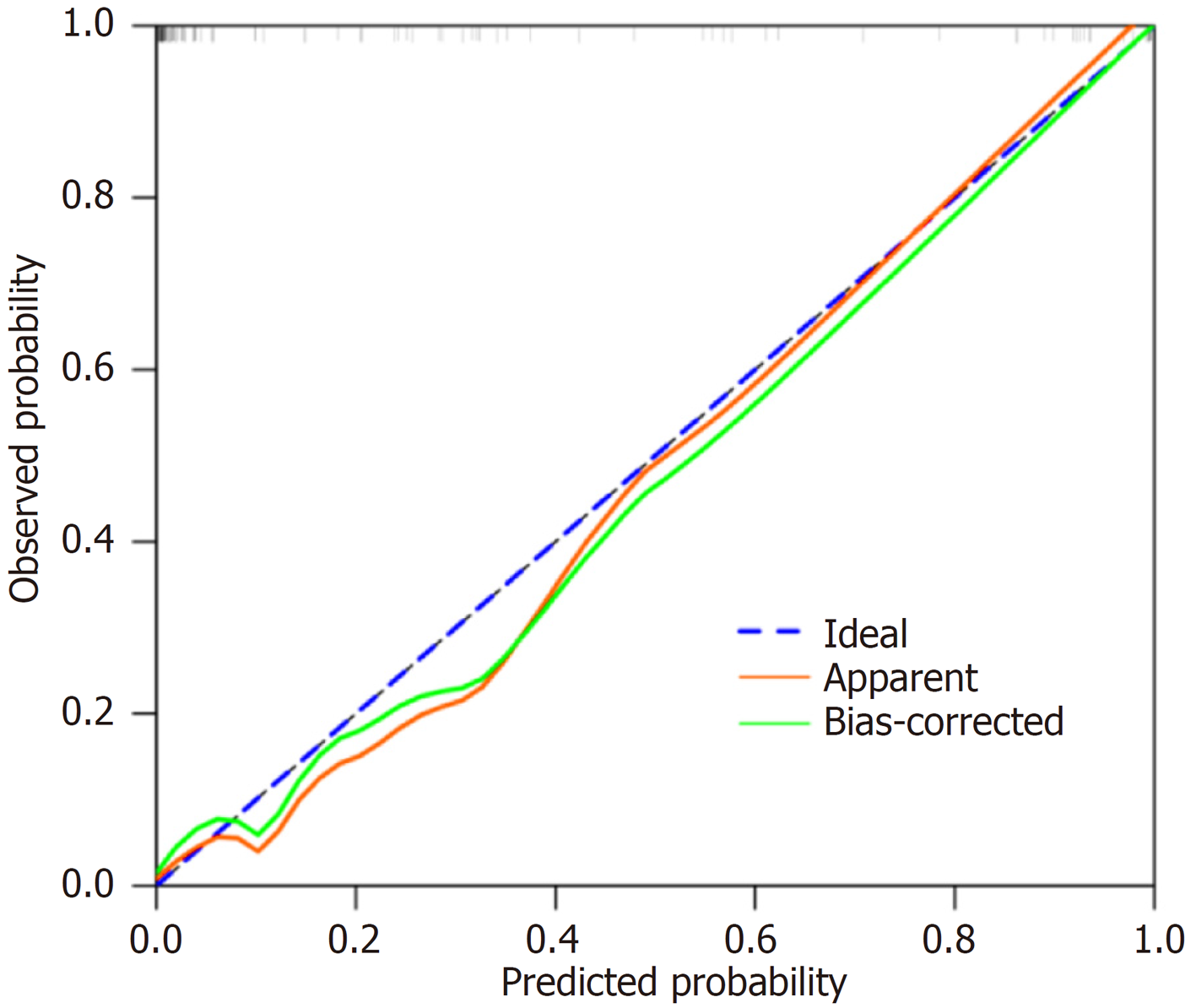
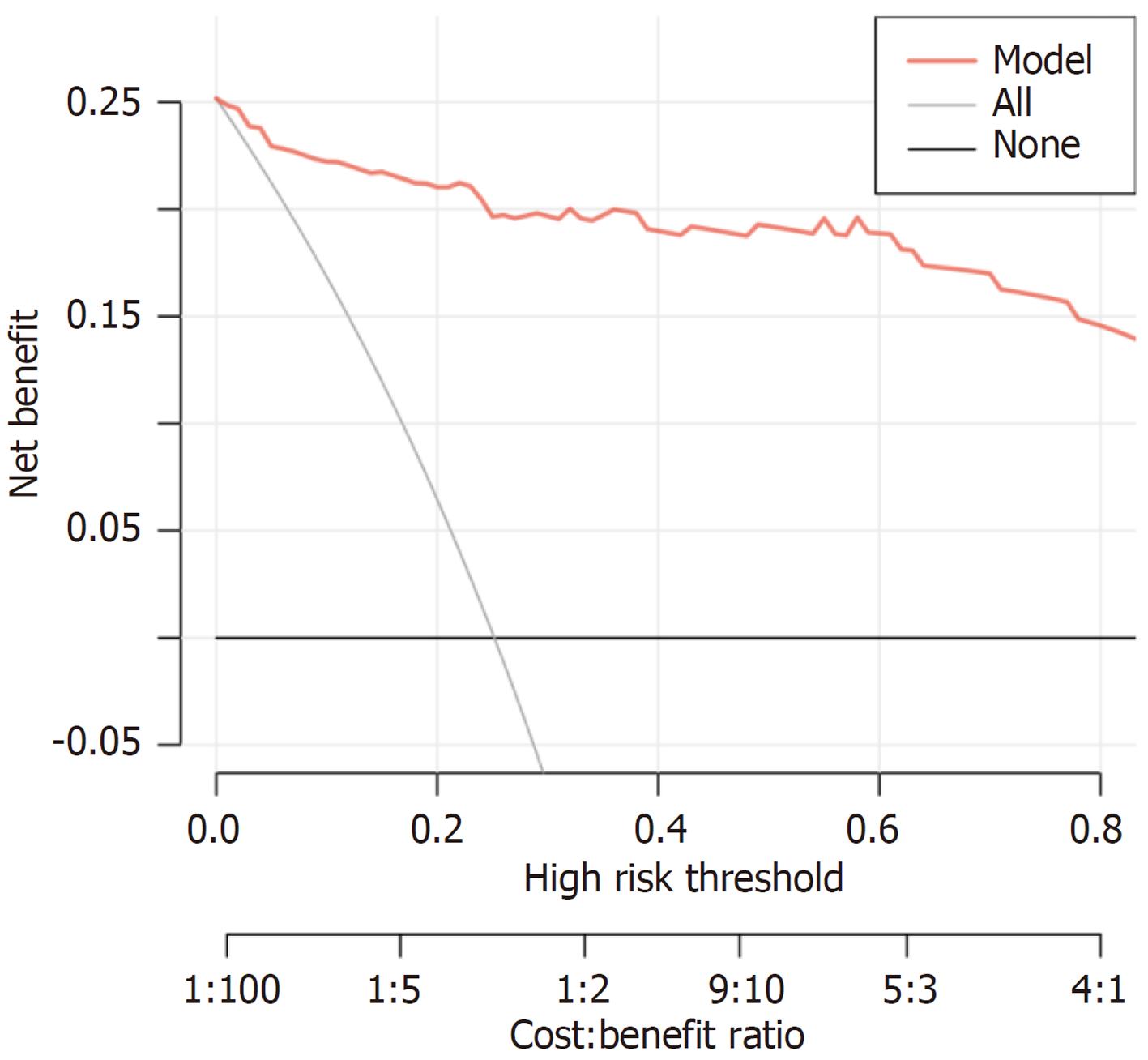
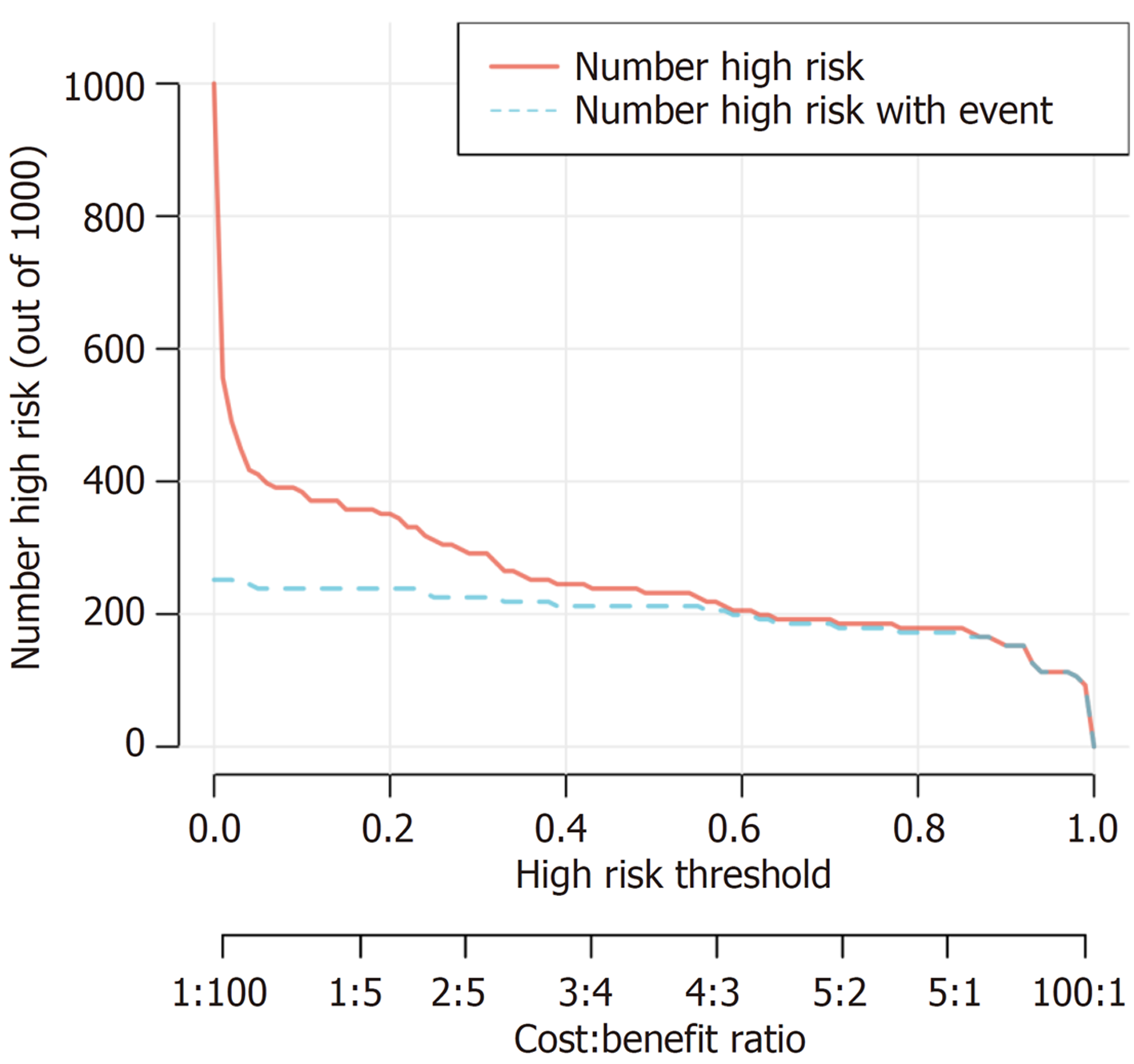
列线图模型的ROC曲线下面积为0.975(95%CI: 0.953-0.998)(图3), 表明模型具有优秀的区分能力. 校准曲线显示, 模型预测的概率与实际观察值之间具有良好的一致性(图4). Hosmer-Lemeshow拟合优度检验结果显示χ2 = 6.2315, P = 0.6213, 进一步证实模型校准良好. 临床决策曲线分析表明, 该列线图模型在较宽的阈值范围内具有较高的净获益, 显示出良好的临床实用价值(图5). 临床影响曲线亦显示模型在高风险人群识别方面具有较好的表现, 曲线在>0.4阈值大部分重合(图6).
随着医学技术的不断发展, ESD已成为治疗早期胃癌的重要手段. 然而, 尽管大多数患者在治疗后能够实现治愈, 仍有部分患者在术后出现复发, 影响了患者的预后并增加了临床治疗的难度[11]. 研究显示[12], H. pylori感染与早期胃癌术后复发之间存在紧密联系. H. pylori通过分泌空泡毒素等物质, 促进胃酸分泌、破坏胃黏膜屏障并激活炎症反应, 这些机制加重了胃黏膜病变并提高了复发的风险. 因此, 识别与H. pylori感染相关的术后复发风险因素并建立有效的预测模型, 对于提高患者的预后和减少术后复发至关重要.
本研究采用Lasso回归进行变量初筛, 旨在从多因素中筛选具有潜在预测价值的候选变量, 但Lasso筛选结果并不代表所有变量均为独立危险因素. 在进一步的多因素Logistic回归分析中, 仅部分变量具有统计学意义, 这提示部分变量可能受到混杂因素或共线性影响. 因此, 本研究最终选择具有统计学意义的5个变量构建列线图模型, 以提高模型的稳定性和临床实用性. 其中, 结果显示, 家族肿瘤史、肿瘤直径、分化程度、CA724及G-17为H. pylori感染早期胃癌患者ESD术后复发的独立危险因素. 分析结果表明, 这些因素的组合对术后复发具有良好的预测价值. 具体而言, 分化程度中低分化的患者由于肿瘤细胞异质性较高, 生物学行为更具侵袭性, 术后复发风险相对增加[13]. 同时, 肿瘤直径较大提示病灶范围更广, 可能存在潜在残留或微小转移, 从而增加复发风险. 血清学指标方面[14], CA724及G-17水平升高可能反映胃黏膜病变活动性增强及肿瘤负荷增加, 与复发风险密切相关. 此外, 具有家族肿瘤史的患者可能存在遗传易感性, 其肿瘤发生发展更为复杂, 亦可能增加术后复发的风险[15,16].
CA724是一种常见的癌胚抗原, 其过表达与肿瘤的恶性生物学行为密切相关, 尤其与肿瘤的浸润、转移及复发相关[17,18]. NLR作为反映全身炎症反应的指标, 其升高与肿瘤的免疫逃逸和复发密切相关[19,20]. G-17作为胃肠激素之一, 能促进胃酸分泌并调节胃黏膜功能, 其异常表达与胃癌的发生和复发密切相关[21,22].
本研究中3年复发率约为25%, 略高于部分既往研究报道水平. 分析其原因可能包括以下几点: 首先, 本研究纳入对象均为H. pylori感染患者, 而持续H. pylori感染被认为与胃黏膜炎症反应及癌前病变进展密切相关, 可能增加异时复发风险; 其次, 本研究将原位复发及异时复发均纳入复发终点, 而部分研究仅统计局部复发, 导致复发率存在差异; 再次, 本研究纳入的患者中部分具有中低分化、肿瘤直径较大等高危特征, 也可能提高总体复发风险. 因此, 本研究复发率虽相对较高, 但具有一定临床合理性.
基于这些独立危险因素, 我们进一步构建了一个术后复发的列线图预测模型. 该模型能够根据患者的临床指标预测术后复发的风险, 并具有较好的预测效能. 通过ROC曲线和校准曲线验证, 模型的预测结果与实际观察值具有较高的一致性, 显示出其较强的临床应用价值. 未来的研究可以进一步扩大样本量并在多中心进行验证, 以提升模型的外部有效性和可靠性.
尽管本研究已成功构建了预测复发的模型, 但仍存在一定的局限性. 首先, 本研究为单中心回顾性分析, 结果可能受到样本选择和数据偏倚的影响. 其次, 模型的外部验证和临床试验尚未进行, 结果的广泛适用性和稳定性需要进一步的评估. 因此, 未来的研究应继续优化模型, 进行更大规模的多中心前瞻性验证, 以进一步提高其预测效能并确保其在临床中的应用.
综上所述, 分化程度中低分化、Ki-67阳性≥50%、H. pylori转阴失败、CA724、NLR、TGFBI和G-17均为H. pylori感染早期胃癌患者ESD术后复发的独立危险因素. 基于这些因素构建的列线图预测模型, 在临床中具有较好的预测价值和应用前景, 可辅助识别高风险患者, 并指导临床干预, 从而降低复发率并改善患者预后. 然而, 未来研究仍需进一步验证模型的外部效度, 优化其预测性能, 并探索更多潜在的风险因素.
尽管早期胃癌患者内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)术后复发的相关研究已逐步开展, 但仍存在一些挑战, 尤其是如何有效预测术后复发的高危因素, 以便在临床中采取针对性防控措施, 从而降低复发率.
体质量指数、年龄及胃泌素17(gastrin-17, G-17)的异常表达等因素与早期胃癌患者ESD术后复发独立相关. 然而, 目前关于早期胃癌患者ESD术后复发的风险预测研究较为有限, 大多数研究侧重于影响因素分析, 缺少相关预测模型的构建.
本研究旨在探讨幽门螺杆菌(Helicobacter pylori, H. pylori)感染早期胃癌患者内镜黏膜下剥离术ESD后复发的危险因素, 并构建预测模型.
回顾性分析接受ESD治疗的152例. H. pylori感染早期胃癌患者的临床资料, 术后3年随访结果. 筛选出与术后复发相关的潜在预测因子, 并根据这些因子构建复发预测模型. 使用受试者工作特征曲线(receiver operating characteristic, ROC)、校准曲线和决策曲线验证模型的预测效能.
通过构建的列线图预测模型, ROC曲线下面积为0.975, 模型的预测值与实际值一致性较高, 具有良好的临床应用价值.
基于实验中的危险因素构建的列线图预测模型, 具有良好的临床预测价值, 可辅助识别高风险患者并指导临床干预, 降低复发率并改善预后.
肿瘤直径较大提示病灶范围更广, 可能增加复发风险. 糖类抗原724及G-17水平升高可能反映胃黏膜病变活动性增强及肿瘤负荷增加, 与复发风险密切相关. 具有家族肿瘤史的患者可能存在遗传易感性, 其肿瘤发生发展更为复杂, 亦可能增加术后复发的风险.
| 1. | Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021;71:209-249. [PubMed] [DOI] |
| 2. | Ferlay J, Colombet M, Soerjomataram I, Parkin DM, Piñeros M, Znaor A, Bray F. Cancer statistics for the year 2020: An overview. Int J Cancer. 2021. [PubMed] [DOI] |
| 3. | Ilic M, Ilic I. Epidemiology of stomach cancer. World J Gastroenterol. 2022;28:1187-1203. [PubMed] [DOI] |
| 4. | Chen Y, Cao Y, Zhi L, Huang R. Endoscopic submucosal dissection combined surgery for the treatment of ectopic gastric mucosa and ectopic pancreas in muscularis propria and serosal layer of the stomach: A rare case report and review of the literature. Medicine (Baltimore). 2025;104:e41297. [PubMed] [DOI] |
| 5. | Hiramatsu T, Kakushima N, Suzuki H, Takizawa K, Hirasawa T, Takeuchi Y, Ishido K, Hoteya S, Yano T, Tanaka S, Toya Y, Nakagawa M, Yoshizaki T, Yoshida N, Hirasawa K, Matsuda M, Yamamoto H, Yokoi C, Ohnita K, Hisanaga Y, Shimazu T, Ono H, Tanabe S, Kondo H, Iishi H, Ninomiya M, Oda I. Outcomes of endoscopic submucosal dissection for locally recurrent early gastric cancer after endoscopic resection: analysis of a multicenter prospective cohort study. Gastric Cancer. 2026;29:169-176. [PubMed] [DOI] |
| 6. | Kim YI, Lee JY, Kim CG, Choi IJ. Helicobacter pylori Infection and Metachronous Gastric Cancer in Elderly Patients With Gastric Cancer Aged ≥ 75 Years Who Underwent Endoscopic Submucosal Dissection. Helicobacter. 2025;30:e70068. [PubMed] [DOI] |
| 7. | Zhang P, Ma X, Tian Z, Cui Z, Zhang Z, Mao T. Prognostic model for early gastric cardia cancer after endoscopic submucosal dissection. BMC Surg. 2025;25:512. [PubMed] [DOI] |
| 8. | 吉 栋德, 段 旭红, 荣 光宏, 逯 艳艳, 李 晓林, 薛 晓红, 许 国彩, 安 玲, 刘 芝兰. 内镜黏膜下剥离术治疗早期胃癌术后复发的相关因素分析. 中国内镜杂志. 2022;28:66-71. [DOI] |
| 9. | Shang X, Zhao Y, Xu T, Ma Q, Su Z. Differential value of PGI, PGII and G-17 in chronic atrophic gastritis and early gastric cancer. Minerva Pediatr (Torino). 2023;75:753-755. [PubMed] [DOI] |
| 11. | Zhang YM, Zhu N, Chen MY, Li FL, Qin B, Jiang J, Wang SH, Wu J, Quan XJ, Wang CY, Zheng Y, Zou BC. Clinical features of early esophageal neoplastic lesions at different stages and efficacy and prognosis after endoscopic submucosal dissection. World J Gastroenterol. 2025;31:110557. [PubMed] [DOI] |
| 12. | Huh CW, Jung DH, Kim JH, Park H, Youn YH. Early versus Late Eradication of Helicobacter pylori after Endoscopic Submucosal Dissection of Gastric Neoplasms: A Prospective, Multicenter, Randomized, Controlled Study. Gut Liver. 2025;19:821-828. [PubMed] [DOI] |
| 14. | Razmi M, Tajik F, Hashemi F, Yazdanpanah A, Hashemi-Niasari F, Divsalar A. The Prognostic Importance of Ki-67 in Gastrointestinal Carcinomas: A Meta-analysis and Multi-omics Approach. J Gastrointest Cancer. 2024;55:599-624. [PubMed] [DOI] |
| 15. | Li S, Nahar A, Zhang Q, Xing J, Li P, Zhang S, Sun X. Risk factors and a nomogram for predicting local recurrence in adult patients with early gastric cancer after endoscopic submucosal dissection. Dig Liver Dis. 2024;56:1921-1929. [PubMed] [DOI] |
| 16. | Wu R, Yang T, Shi L, Ding X, Dou X, Wang Y, Chen M, Wang L, Xu G, Zou X, Zhang W. Helicobacter pylori infection increases risk of bleeding during endoscopic submucosal dissection for early gastric cancer. Surg Endosc. 2024;38:7287-7297. [PubMed] [DOI] |
| 17. | Sun A, Chen H, Shi X, Shang Z, Zhang J. Diagnostic Value of Joint Detection of Serum TK1, TSGF, CA199, and CA724 for Gastric Cancer and Its Relationship With Clinicopathologic Features and Prognosis. Am Surg. 2025;91:570-578. [PubMed] [DOI] |
| 18. | Zhou CM, Zhao SH. Evaluation of the value of combined detection of tumor markers CA724, carcinoembryonic antigen, CA242, and CA19-9 in gastric cancer. World J Gastrointest Oncol. 2024;16:1737-1744. [PubMed] [DOI] |
| 19. | Maloney S, Pavlakis N, Itchins M, Arena J, Mittal A, Hudson A, Colvin E, Sahni S, Diakos C, Chan D, Gill AJ, Samra J, Clarke SJ. The Prognostic and Predictive Role of the Neutrophil-to-Lymphocyte Ratio (NLR), Platelet-to-Lymphocyte Ratio (PLR), and Lymphocyte-to-Monocyte Ratio (LMR) as Biomarkers in Resected Pancreatic Cancer. J Clin Med. 2023;12:1989. [PubMed] [DOI] |
| 20. | Hayashi H, Yasufuku I, Sato Y, Fujibayashi S, Chikaishi W, Endo M, Horaguchi T, Yokoi R, Matsumoto K, Kuno M, Sengoku Y, Fukada M, Asai R, Tajima JY, Makiyama A, Kiyama S, Tanaka Y, Murase K, Ishihara T, Matsuhashi N. Neutrophiltolymphocyte ratio and risk of disease progression in patients with nivolumabtreated unresectable or recurrent gastric cancer. Oncol Lett. 2025;29:20. [PubMed] [DOI] |
| 21. | Zhang T, Zhou X, Meng X, Li J, Hou S, Wang J, Yin M, Cao L, Wang B. The potential value of serum pepsinogen and gastrin-17 for the diagnosis of chronic atrophic gastritis at different stages of severity: a clinical diagnostic study. BMC Gastroenterol. 2025;25:428. [PubMed] [DOI] |
| 22. | Xiao M, Zhang Z, Liao G, Liu M, Chen X. Analysis of the Value of Helicobacter pylori Test in Combination with the Determination of Plasma Propepsin and Gastrin 17 in Screening the Precancerous Status of Gastric Cancer. Cell Mol Biol (Noisy-le-grand). 2022;68:110-115. [PubMed] [DOI] |
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C
D级 (一般): 0
E级 (差): E
科学编辑: 刘继红 制作编辑:张砚梁