修回日期: 2026-03-19
接受日期: 2026-03-25
在线出版日期: 2026-03-28
结直肠癌(colorectal cancer, CRC)作为全球高发的消化道恶性肿瘤, 其发生发展遵循"正常黏膜-腺瘤-腺癌"的经典序列, 研究表明约80%的CRC患者符合这一规律, 从腺瘤性息肉到侵袭性癌的平均时间窗口为5-10年, 这为通过早期筛查实施干预提供了关键窗口. 然而, 传统依赖结肠镜或粪便隐血试验的筛查模式, 因依从性低、资源不均及对早期病变灵敏度相对不足而面临瓶颈. 当前, 筛查技术正迎来深刻变革: 多靶点粪便DNA检测、基于血液游离DNA甲基化的液体活检等非侵入性分子诊断技术不断突破, 与人工智能辅助结肠镜相结合, 显著提升了筛查的精准性与可及性. 本文系统评述了结直肠癌筛查的技术进展, 并论证其核心在于依托多技术集成与全流程模式优化, 以构建智能防控体系. 文章阐述了通过优化关键环节提升体系效能的具体路径, 并分析了本土化实施的主要挑战, 旨在为全面提升筛查成效提供参考.
核心提要: 结直肠癌筛查正从单一检测转向"社区初筛-风险分层-结肠镜精筛-智能随访"的全流程智能防控新范式. 它整合多靶点粪便DNA、液体活检与人工智能辅助结肠镜, 系统性破解精准性、可及性与成本效益瓶颈, 推动从疾病检测向主动健康管理转变.
引文著录: 任丹, 崔曼莉, 张明鑫. 结直肠癌筛查技术创新发展: 从单一检测到全流程智能防控体系构建. 世界华人消化杂志 2026; 34(3): 220-228
Revised: March 19, 2026
Accepted: March 25, 2026
Published online: March 28, 2026
Colorectal cancer (CRC), a highly prevalent malignant tumor of the digestive tract worldwide, develops via the classic "normal mucosa-adenoma-carcinoma" sequence. Studies indicate that approximately 80% of CRC cases follow this pattern. The mean time window from adenomatous polyps to invasive carcinoma is 5-10 years, which provides a critical opportunity for intervention through early screening. However, the traditional screening paradigm, primarily reliant on colonoscopy and the fecal immunochemical test, is constrained by several critical bottlenecks: Low population adherence, uneven distribution of healthcare resources, and insufficient sensitivity for detecting early-stage lesions. Currently, screening technologies are undergoing profound transformation: Breakthroughs in noninvasive molecular diagnostic techniques, such as multitarget stool DNA testing and bloodbased liquid biopsy analyzing cell-free DNA methylation, combined with artificial intelligenceassisted colonoscopy, are significantly enhancing both the precision and accessibility of screening. This article systematically reviews the technological advances in CRC screening and argues that the core lies in relying on the integration of multiple technologies and the optimization of the entire process to build an intelligent prevention and control system. It elucidates the specific pathways for enhancing the system's efficiency by optimizing key steps and analyzes the main challenges of its localized implementation, aiming to provide a reference for comprehensively improving screening outcomes.
- Citation: Ren D, Cui ML, Zhang MX. Colorectal cancer screening: Technological innovation from single modality testing to a comprehensive intelligent prevention and control system. Shijie Huaren Xiaohua Zazhi 2026; 34(3): 220-228
- URL: https://www.wjgnet.com/1009-3079/full/v34/i3/220.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v34.i3.220
核心提要: 结直肠癌筛查正从单一检测转向"社区初筛-风险分层-结肠镜精筛-智能随访"的全流程智能防控新范式. 它整合多靶点粪便DNA、液体活检与人工智能辅助结肠镜, 系统性破解精准性、可及性与成本效益瓶颈, 推动从疾病检测向主动健康管理转变.
结直肠癌(colorectal cancer, CRC)是严重威胁人类健康的消化道恶性肿瘤, 其全球发病率高居肿瘤第三位, 死亡率位居第二, 已成为重大的全球性公共卫生挑战[1]. 在我国, 这一形势尤为严峻, 据国家癌症中心最新统计数据显示, 2022年我国CRC新发病例约52万, 死亡病例约24万, 发病率与死亡率在恶性肿瘤分别位列第2位和第4位, 疾病负担沉重且持续加重[2]. 随着人们生活水平的不断提高以及生活方式的改变, 尤其是膳食结构的改变, CRC的发病率和死亡率呈明显上升趋势[3]. CRC的发展通常历时5-10年, 这为早期筛查和干预提供了关键窗口期[4]. 已知在全球范围内, CRC的5年生存率普遍较低, 而在中国这一情况尤为严重[5]. 研究表明[6], 早期CRC患者5年生存率可高达90%-95%, 而晚期存活率不足10%. 近年来我国CRC患者5年生存率虽有所提高, 但仍处于较低水平, 如早期发现、早期治疗, 将使5年生存率显著提高[7]. 鉴于以上特点, 世界卫生组织已将其列为最适合实施人群早期筛查以及预防的癌症种类之一. 因此, 早期筛查是有效降低CRC死亡率、挽救生命的决定性手段. 美国的成功实践为此提供了有力佐证: 通过普及筛查和控制风险因素, 癌症总体死亡率自1991年峰值以来下降了34%[8], 其中CRC筛查的普及贡献显著, 这充分证明了筛查作为公共卫生干预措施的巨大价值, 也激励着筛查技术的不断创新与模式的优化.
现有筛查主要依赖于结肠镜和粪便潜血试验等技术. 结肠镜虽是诊断的"金标准", 但其作为初筛手段存在侵入性强、肠道准备繁琐、医疗资源消耗大及人群依从性低等局限; 而传统的粪便潜血试验则对早期病变和癌前病变的检测灵敏度有限[9]. 在此背景下, CRC筛查领域正迎来深刻的技术革新. 多靶点粪便DNA检测、基于血液循环肿瘤DNA(circulating tumor DNA, ctDNA)甲基化的液体活检等新型分子标志物不断涌现, 与人工智能辅助结肠镜诊断等前沿技术相结合, 显著提升了筛查的精准性与便捷性. 这些技术进步正在推动筛查模式的深刻变革. 其核心方向是从依赖单一技术, 转向多技术集成与全流程模式优化, 以实现筛查效率与效益的系统性提升. 本文旨在系统评述CRC筛查从非侵入性分子诊断到人工智能赋能的技术进展, 并重点探讨如何优化"社区初筛-风险分层-结肠镜精筛-智能随访"这一全路径中的关键环节, 以构建更高效、更具弹性的智能防控体系.
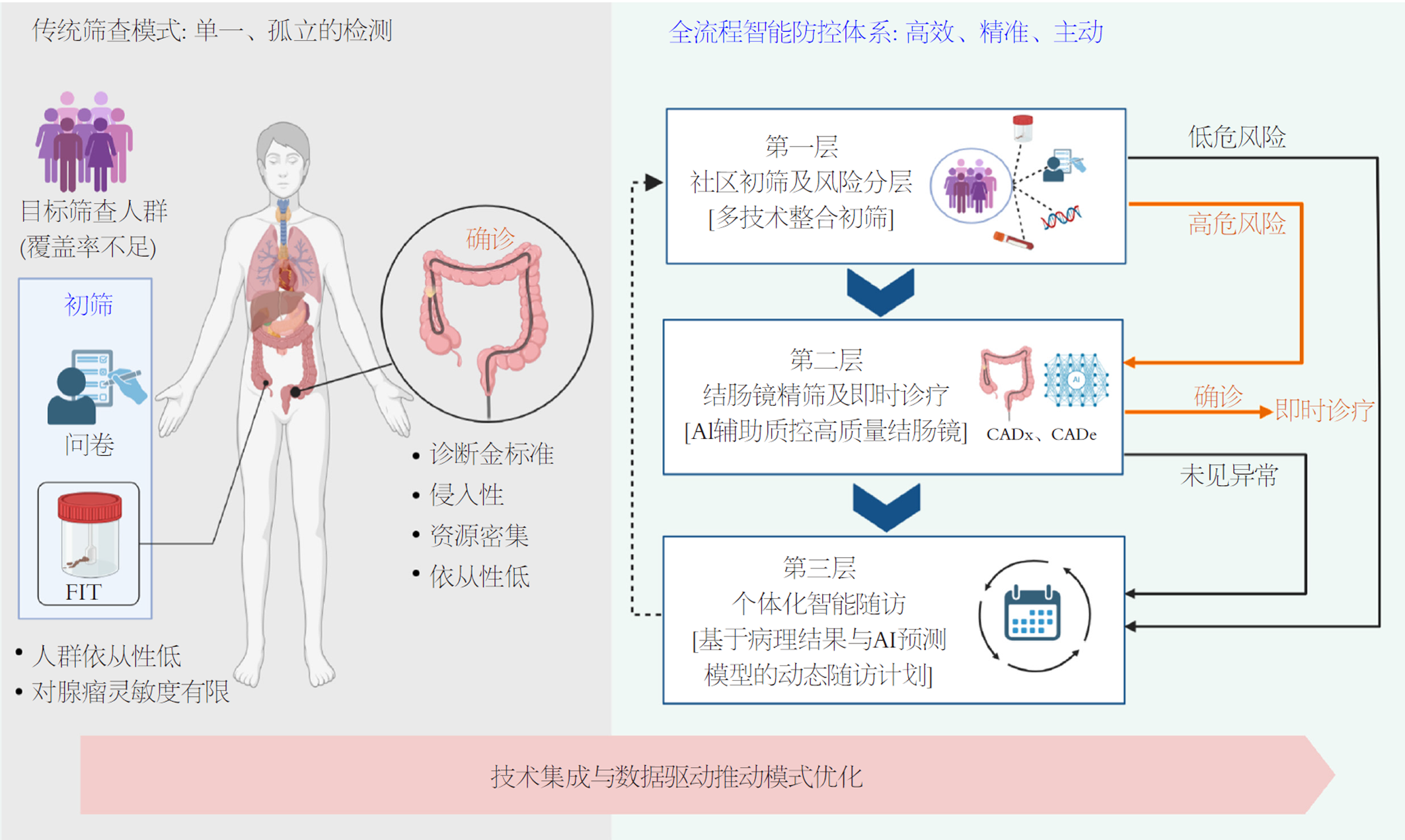
CRC筛查正经历从传统单一模式, 向依托技术集成与模式优化的全流程智能防控体系的深刻变革(图1).
此类技术通过检测肿瘤释放到体液中的生物标志物实现"无创"筛查, 极大提升了筛查的可及性与人群接受度, 是实现筛查"关口前移"的核心(见表1).
| 技术类别 | 核心特点与原理 | 主要优势 | 体系中的角色 |
| 粪便免疫化学检测 | 通过检测粪便血红蛋白进行初筛, 操作简便 | 成本最低, 易于大规模部署 | 社区初筛的基石, 用于广泛覆盖与初步分流 |
| 多靶点粪便DNA检测 | 整合多种分子标志物(如基因突变、甲基化), 实现更精准的分子检测 | 对癌及癌前病变的综合检出能力最强 | 精准初筛与风险分层的关键工具 |
| 血液液体活检 | 通过抽血分析血液中的循环肿瘤DNA等标志物 | 采样便捷, 患者接受度最高 | 重要的"替代路径", 提升筛查可及性 |
| 尿液代谢组学 | 分析尿液中的特征性代谢物谱, 完全无创 | 采样最方便, 用户体验佳 | 前沿探索方向, 未来无创筛查的潜在方向 |
| 人工智能辅助诊断 | 基于深度学习算法实时分析内镜图像, 辅助识别病灶 | 提升息肉检出率, 实现操作质量标准化 | "结肠镜精筛"环节的质量增强器 |
1.1.1 基于粪便标志物的检测: 基于粪便的CRC筛查技术已从传统的隐血检测发展为多组学整合的筛查体系. 粪便免疫化学测试(fecal immunochemical test, FIT)因其简便、经济且在降低CRC发病率和死亡率方面证据明确, 仍是许多国家有组织筛查项目的基石, 其筛查间期通常为1-2年. 最新的大规模随机对照试验(COLONPREV试验)证实, 在降低CRC死亡率方面, 基于FIT的筛查程序不劣于基于结肠镜的程序, 这主要得益于其更高的参与率[10].
多靶点粪便FIT-DNA检测是通过整合基因突变(如KRAS)、甲基化标志物(如NDRG4、BMP3)和FIT, 显著提升了筛查效能[11]. 初代检测技术对CRC的敏感度达92.3%, 对进展期腺瘤的敏感度为42.4%[12]. 新一代多靶点粪便DNA检测进一步优化了性能, 其包括了DNA分子标志物和血红蛋白水平评估, 旨在提升CRC筛查的特异性, 结果显示其对CRC的敏感度提升至93.9%, 对进展期腺瘤的敏感度为43.4%, 特异性也提高至90.6%, 显示出更优的筛查效益[13]. 该技术已获得美国FDA的批准, 推荐用于平均风险人群的3年一次筛查.
粪便DNA甲基化检测作为一种更稳定、成本更低的替代方案, 显示出巨大潜力. 其主要标志物为黏结蛋白聚糖2(syndecan-2, SDC2)基因的甲基化[14], 研究表明[15], 基于SDC2甲基化检测结果显示83.8%的敏感度和98.0%的特异性, 显示出良好的检测性能. 另外, SEPT9(septin9)基因甲基化检测敏感度也可达97.2%[16]. 多基因联合检测可进一步提升性能, 例如: SDC2与组织因子途径抑制剂(tissue factor pathway inhibitor 2, TFPI2)联合检测的曲线下面积达0.913, 显著高于单独检测的效果[17]. SDC2、TFPI2与分泌型卷曲相关蛋白三基因联合检测的特异性达86.7%[18]. 与需要全量粪便样本且处理时间紧迫的多靶点检测相比, 甲基化检测仅需1-2克粪便, 样本稳定性更高(可保存4 wk), 在成本和操作简便性上更适用于大规模人群筛查[19].
除DNA标志物外, 粪便RNA标志物, 包括mRNA、miRNA(如miR-135b-5p)和长链非编码RNA(long noncoding RNAs, lncRNA)(如CCAT1、CCAT2), 也呈现出特异性表达谱[20-22]. 蛋白质组学研究发现多个具有诊断价值的粪便蛋白标志物, 如补体C3、乳铁蛋白等组成的标志物组合在95%特异性下达到80%的敏感度[9,23]. 挥发性有机物分析显示丙酮醇等特定VOCs在CRC患者粪便中含量显著升高, 联合检测敏感度可达87.9%[24]. 微生物组分析表明梭菌等特定菌群在CRC患者粪便中丰度异常, 为筛查提供了新的生物标志物[25].
这些技术进步共同推动了CRC筛查从单一标志物检测向多组学整合的方向发展, 为构建精准筛查体系奠定了基础. 未来通过高通量技术发现新标志物并开展多中心临床验证, 将进一步提升粪便筛查的临床应用价值.
1.1.2 基于血液标志物的检测: 液体活检是一种基于血液的检测方式, 旨在检测与肿瘤相关的成分, 包括循环肿瘤DNA、肿瘤细胞和细胞外囊泡[26]. 其中, 来源于恶性细胞的ctDNA以及来源于正常组织和癌组织的无细胞DNA(cell-free DNA, cfDNA)是CRC检测的主要目标[27].
在ctDNA检测中, DNA甲基化是关键的表观遗传学标志物, 临床上最常见的是SEPT9基因甲基化(mSEPT9)[28]. 根据已有研究显示, mSEPT9基因已被批准用于CRC的早期诊断[29], 大规模临床试验结果显示, mSEPT9在检测CRC的灵敏度和特异度分别为74.8%和87.4%, 均显著优于FIT的水平, 为不愿接受粪便检测的人群提供了有效选择[30].
近年来, CRC早期液体活检技术取得显著进展, 在多类生物标志物研究中展现出良好潜力. 例如, 基于NTMT1和MAP3K14-AS1的cfDNA检测对早期CRC(Ⅰ/Ⅱ期)的灵敏度达87.4%, 对晚期腺瘤的灵敏度为43.5%[31]. 进一步的研究[32]则筛选出更具潜力的组合: 一项多中心研究在其验证队列中发现, 血清cfDNA中GALNT9和UPF3A的甲基化组合检测晚期腺瘤和CRC的敏感度达78.8%, 特异度为100%, 其综合诊断效能优于传统FIT和SEPT9检测. 此外, 一种涵盖11个甲基化标志物的cfDNA检测模型亦被报道, 其对早期CRC和晚期腺瘤均展现出高敏感性与特异性[33,34].
除甲基化标志物外, 液体活检的研究已拓展至多组学范畴. 蛋白质组学研究发现, 外泌体蛋白QSOX1在CRC患者血浆中表达显著降低[35], 而血清标志物ROBO4与PCDH12则表达升高, 两者联合检测的曲线下面积可达0.812, 诊断效能优于传统肿瘤标志物CEA和CA199[36]. 在非编码RNA方面, 环状RNA成为新兴标志物, 研究证实, 如hsa_circ_0049487等环状RNA在腺瘤阶段即发生显著改变, 其对癌前病变的识别能力优异[37,38]. 而lncRNA如LOC285194、RP11462C24.1等构建的联合检测模型, 其诊断效能亦优于传统CEA标志物[39].
尽管血清标志物具有无创、便捷等优势, 但仍面临标准化不足、大规模人群验证缺乏等挑战. 未来需通过多组学整合与人工智能分析, 进一步提升对早期病变的识别能力, 推动其在规模化筛查中的应用.
1.1.3 基于尿液标志物的检测: 尿液代谢组学作为CRC无创筛查的新兴方向, 通过液相色谱-质谱法等技术分析尿液代谢谱, 识别与肿瘤相关的特征性代谢指纹. 初步研究显示, 特定代谢物组合(如二乙酰精胺与犬尿氨酸)诊断CRC的敏感度与特异度均可达80.0%[40]; 另有研究提示, 包含牛磺酸、丙氨酸等的代谢谱对晚期腺瘤识别敏感度达75%、特异性达100%, 展现出对癌前病变的预警潜力[41]. 目前该技术仍处研究阶段, 敏感度与特异性尚不稳定, 缺乏大规模前瞻性研究验证, 未来需标准化检测流程并明确其临床定位.
综上, 非侵入性分子诊断技术已形成多元发展格局. 传统FIT因其经济性与便捷性, 仍是大规模人群初筛的基石; 多靶点粪便DNA检测凭借对进展期腺瘤更高的灵敏度, 成为精准初筛的重要工具; 血液液体活检为抗拒粪便检测者提供了关键替代路径; 而尿液检测等新兴技术则是未来无创筛查的潜在方向. 这些技术共同构成了全流程智能防控体系中初筛与风险分层环节的"技术工具箱", 为实现精准分流奠定了坚实基础.
近年来, 人工智能(artificial intelligence, AI)技术, 特别是基于深度学习的计算机辅助检测(computer-aided detection, CADe)和诊断系统, 已从概念验证快速迈向临床常规应用, 成为CRC筛查领域最具变革性的技术方向.
1.2.1 实时检测系统的临床验证: 多项大规模随机对照试验为AI辅助结肠镜的有效性提供了高级别循证依据. 2020年Repici等[42]开展的里程碑式研究显示, CADe将腺瘤检出率(adenoma detection rate, ADR)从40.4%提升至54.8%. 此后, Xu等[43]在中国3059例患者中验证了这一效果, 而Seager等[44]的COLO-DETECT研究进一步在真实世界环境中证实了AI的实效性. 2025年一项中国多中心RCT进一步验证了国产AI系统在提升息肉检出率、尤其是改善≤5 mm小息肉和扁平息肉检出方面的显著效果[45].
1.2.2 漏诊率降低与质量标准化: AI的核心价值在于减少人为因素导致的漏诊, Wallace等[46]的研究显示, CADe使腺瘤漏诊率相对降低了约52%[46], 这一改善主要归因于AI对视野内已存在但未被医师识别的病灶的捕捉能力. 此外, AI系统可自动记录退镜时间、肠道准备质量等关键质控指标, 推动筛查标准化[47].
此外, 人工智能的赋能正从"结果辅助"向"过程优化"深度拓展. 最新前瞻性研究引入了由AI视频分析定义的"有效退镜时间"(effective withdrawal time, EWT)-即内镜下清晰、稳定观察黏膜的真实时间. 研究表明[48], EWT是比传统退镜时间(standard withdrawal time, SWT)更强大的腺瘤检出预测因子(EWT每增加1 min, ADR显著升高), 而传统SWT中约40%的时间被AI判定为无效操作. 这揭示, AI能够通过客观量化操作过程的核心质量, 为内镜医师提供超越主观经验的精准反馈, 从而推动结肠镜检查从"时间达标"到"有效观察时间"最大化的质控范式转变, 从根源上提升筛查质量并降低间期癌风险.
1.2.3 深度学习架构的技术演进: 技术层面, AI模型正从传统卷积神经网络向Mamba等高效架构演进[49], 通过选择性状态空间机制在保持线性计算复杂度的同时提升特征提取效率[50]. 2025年, 中国多中心随机对照试验验证的国产CADe系统通过优化特征金字塔网络, 在实时检测条件下(<50 ms延迟)将息肉检出率提升至显著水平, 尤其对≤5 mm微小息肉和扁平息肉的检出改善明显[45].
1.2.4 风险预测与筛查分层: 超越内镜实时辅助, AI正拓展至筛查风险分层. 2025年最新研究利用常规全血细胞计数数据, 通过Transformer模型(TabPFN)实现CRC风险预筛查, 虽灵敏度(64%)低于FIT(88%), 但特异性更优(81% vs 77%), 且无需专门采样, 极具人群筛查成本效益潜力[51]. 同时, 前沿共识指出, 利用AI整合粪便中的宿主DNA甲基化与肠道微生物组等多组学信号, 有望将晚期癌前病变的检测灵敏度提升至55%-65%(特异性~94%), 代表了从"癌症检测"迈向"癌症预防"的精准筛查新范式[52]. 人工智能的风险分层与优化效能进一步延伸至病理诊断环节. 最新研究表明, 基于深度学习的数字病理系统能够对结肠息肉活检切片进行精准预筛查, 在确保诊断安全的前提下(对癌及高级别病变的识别敏感度>98%), 可准确识别出超过83%的低风险病例, 从而将病理专家的工作负荷聚焦于最具挑战性的病变上[53]. 这实现了在诊断端对医疗资源的智能再分配, 构成了从"社区初筛"到"病理精诊"的全流程智能防控体系的关键一环.
尽管证据迅速积累, AI筛查仍面临挑战. 2025年英国医学杂志社论指出[54], CADe的临床效益可能被高估, 需关注假阳性导致的过度活检和成本效益问题. 欧洲消化内镜学会2025年立场声明强调, 标准化培训是安全有效应用AI的前提[55]. 未来方向包括AI与辅助设备(透明帽、球囊)联合消除皱襞盲区; 可解释AI(Explainable AI)提升临床信任; 以及整合影像-临床-分子数据的多模态模型, 实现从"一刀切"筛查向精准化、个体化预防的转变.
粪便多靶点DNA检测、液体活检以及人工智能等技术的突破, 共同指向了未来筛查模式优化的核心方向: 即如何利用这些工具实现精准分流、质量控制和全程管理.
技术的迭代不仅提升了单项检测的性能, 更为筛查模式的深刻变革提供了动力. 为系统应对资源有限、参与率不足与质量不均等核心挑战, 构建一个整合"社区初筛-风险分层-结肠镜精筛-智能随访"的全流程智能防控体系已成为重要发展方向. 该体系的构建并非抽象概念的推演, 其核心在于依托关键技术的集成创新, 并对筛查全流程进行切实的模式优化. 因此, 体系的有效性直接体现在以下几个核心环节的优化实践上.
此模式的核心理念是打破"一刀切"的筛查策略, 根据个体风险差异配置不同强度的筛查资源, 其关键在于实现精准的"初筛-分流".
在实践中, 中国的"两步筛查"策略(即风险问卷结合FIT初筛, 阳性者转诊结肠镜)已证明了分层筛查的可行性. 一项多中心随机对照试验证据表明, 这种风险适应型筛查策略(高危人群直接行结肠镜, 低危人群接受FIT)相较于单纯的FIT筛查, 能够实现更高的参与率和进展期肿瘤检出率, 为在资源有限条件下实施分层筛查提供了重要的中国证据[56]. 优化方向在于引入更精准的工具进行风险量化. 例如, 可考虑将定量FIT(血红蛋白浓度)、多靶点粪便DNA检测或基于常规血液指标(如2025年研究提及的基于全血细胞计数的AI模型)构建的风险评分, 作为更精细的初筛分层工具[51], 这将人群划分为低、中、高危等级, 从而差异化安排后续筛查间隔或直接决定是否进入结肠镜精筛.
首先, 在初筛与基础风险分层之后, 可对中危或风险不明确的个体(如FIT阴性但具家族史者), 采用高特异性技术(如血液ctDNA检测)进行二次精筛. 该策略的核心目的是将结肠镜等稀缺诊断资源精准导向风险最高的个体, 以最大化健康产出. 卫生经济学模型研究(如MISCAN-Colon)已为此提供了证据支持, 证实基于风险分层的目标性干预比无差别筛查更具成本效益[57].
其次, 当标准精筛路径(结肠镜)因患者意愿或临床禁忌无法实施时, 体系需具备有效的替代方案以防止筛查链条中断. 对此类人群, 采用高灵敏度粪便DNA检测进行定期监测, 是一项重要的循证支持的替代管理策略. 北加利福尼亚凯撒医疗机构(Kaiser Permanente Northern California, KPNC)通过"提供灵活筛查选择并实施主动随访管理", 将筛查覆盖率提升至82.7%的成功实践, 证明了该策略对于维持人群筛查依从性与体系整体效能的关键作用[58].
此外, 为巩固筛查成效, 需对息肉切除术后患者进行差异化的长期管理. 整合新型分子标志物(如ctDNA)与人工智能进行复发风险预测, 有助于推动监测模式从统一的固定间隔向基于个体复发风险的动态调整模式转变[59]. 这能优化长期随访的资源配置, 避免低风险者的过度检查, 同时强化对高风险者的管理.
人工智能与信息化工具的价值, 应具体体现为对筛查关键环节的赋能, 提升其客观性、规范性与一致性.
个体化决策支持: 整合多源数据(问卷、检验、病史)的AI风险预测模型, 可用于推荐个性化的筛查起始年龄、首选方法与间隔. 例如, 结合初筛定量结果与遗传风险, 动态调整后续检查策略.
结肠镜质量闭环控制: AI在结肠镜中的应用已从辅助发现(CADe)走向质控核心. 随机对照试验(如AQCS研究)证明, 实时监测退镜时间、肠道准备质量的自动质量控制系统能显著提升腺瘤检出率[60]. 同时, 自动化ADR计算平台实现了质量指标的客观、高效评估, 推动质控从"事后抽查"迈向"实时反馈与改进"[61].
智能化随访管理: 信息系统自动根据息肉病理结果生成个体化随访计划, 并通过数字化工具(如自动化提醒)进行主动管理, 这是巩固筛查效果、防止失访的关键. KPNC的成功实践表明, 这种主动管理能极大提升长期参与率和最终健康结局[58].
构成体系的优化模式在中国落地的可行性, 必须结合现实情境进行审慎评估.
卫生经济学与支付政策: 任何新技术(如粪便DNA检测、液体活检)或复杂路径的引入, 都需要严格的成本-效果分析. 其能否被纳入地方或国家层面的筛查项目、医保如何支付, 是决定其可及性的首要因素.
医疗资源与技术可及性: AI辅助诊断系统、一体化信息平台的建设与维护需要相当的投入. 需考虑不同层级医疗机构(特别是基层筛查点)的基础设施差异, 避免因技术升级加剧筛查服务的"数字鸿沟".
数据标准化与隐私安全: 实现跨机构、全流程的数据整合与AI分析, 前提是建立统一的数据标准. 同时, 必须构建符合《个人信息保护法》等法规的严格数据安全与隐私保护框架.
尽管通过技术集成对筛查关键环节进行模式优化的路径已日益清晰, 但将这些具体优化策略转化为大规模、可持续的公共卫生实践, 仍面临多重现实挑战. 未来的发展依赖于技术创新与卫生系统改革的深度融合.
体系的落地主要面临以下几重瓶颈: 首先, 卫生经济学平衡问题, 新型分子检测与AI系统的引入推高了直接成本, 亟需基于大规模人群数据开展成本-效果研究, 以确立最具成本效益的技术整合路径. 其次, 医疗资源的结构性矛盾, 体系高效运转依赖于充足的结肠镜资源与高质量内镜医师, 这与筛查服务下沉基层的诉求存在冲突, 需通过远程医疗、AI辅助培训等手段系统性提升基层服务能力. 最后, 证据向实践的转化鸿沟, 许多AI工具与新型生物标志物仍停留于临床验证阶段, 缺乏在真实世界筛查项目中长期应用的有效性、安全性与公平性数据.
未来, 筛查模式的优化将向更精准、更动态、更融合的方向演进: 一是筛查的彻底个体化, 通过深度融合多组学数据(基因组、表观组、微生物组)、个人可穿戴设备数据及长期电子健康档案, 构建动态的超个性化风险预测与筛查策略模型. 二是技术的深度无缝融合, 下一代体系将实现"液体活检"(提供分子风险信号)与"AI影像"(保障精准解剖诊断)的实时数据交互与决策互补, 并与物联网设备联动, 构建立体健康预警网络. 三是聚焦公平与可及性, 技术发展应致力于缩小筛查差距, 通过开发低成本、易实施的方案, 并设计能够覆盖边缘化人群、消除数字鸿沟的筛查项目, 推动防控效益的广泛共享.
CRC筛查领域正处于一个由技术集成创新驱动发展的关键阶段. 未来筛查效能的提升, 不再仅仅依赖于单项检测技术的突破, 而更在于如何通过系统的模式优化, 将多种技术协同应用于筛查全流程. 本文系统评述了关键的技术进展, 并详细阐述了通过对"社区初筛-风险分层-结肠镜精筛-智能随访"这一路径中关键环节进行优化-即基于风险分层的精准分流、多技术联用以应对复杂场景、以及数据与AI驱动的质量闭环控制-来系统性提升筛查资源配置效率、管理韧性与质量规范性的具体策略.
然而, 上述优化模式的落地同样面临严峻的现实挑战, 包括需严格验证的卫生经济学效益、亟待弥合的医疗资源与数字鸿沟, 以及从临床证据到公共卫生实践的转化壁垒. 因此, CRC筛查的未来发展, 必然是技术创新与卫生系统改革深度融合的过程. 持续推进以证据为基础、以公平可及为导向的筛查模式优化与实践, 是应对这些挑战、切实降低CRC疾病负担、最终实现从"治疗疾病"向"主动健康管理"迈进的核心路径.
| 1. | Bray F, Laversanne M, Sung H, Ferlay J, Siegel RL, Soerjomataram I, Jemal A. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74:229-263. [PubMed] [DOI] |
| 2. | Han B, Zheng R, Zeng H, Wang S, Sun K, Chen R, Li L, Wei W, He J. Cancer incidence and mortality in China, 2022. J Natl Cancer Cent. 2024;4:47-53. [PubMed] [DOI] |
| 3. | Matsuda T, Fujimoto A, Igarashi Y. Colorectal Cancer: Epidemiology, Risk Factors, and Public Health Strategies. Digestion. 2025;106:91-99. [PubMed] [DOI] |
| 4. | Shaukat A, Levin TR. Current and future colorectal cancer screening strategies. Nat Rev Gastroenterol Hepatol. 2022;19:521-531. [PubMed] [DOI] |
| 5. | 宁 思明, 孙 宝, 晋 亚楠, 杨 瑞霞, 齐 冰, 康 晓宇, 乔 逸. 1990-2021年中国结直肠癌疾病负担研究及2022-2041年变化趋势分析. 现代肿瘤医学. 2025;33:1579-1587. [DOI] |
| 7. | Huybrechts I, Kliemann N, Perol O, Cattey-Javouhey A, Benech N, Maire A, Lignini T, Carretier J, Saurin JC, Fervers B, Gunter MJ. Feasibility Study to Assess the Impact of a Lifestyle Intervention during Colorectal Cancer Screening in France. Nutrients. 2021;13:3685. [PubMed] [DOI] |
| 8. | Sansbury BM, Blackman E, Primm KM, Zaidi SK, Sengupta R. AACR Cancer Progress Report 2025: Unifying Cancer Science and Medicine: A Continuum of Innovation for Impact. Clin Cancer Res. 2025;31:4239-4243. [PubMed] [DOI] |
| 9. | Ding Q, Kong X, Zhong W, Liu W. Fecal biomarkers: Non-invasive diagnosis of colorectal cancer. Front Oncol. 2022;12:971930. [PubMed] [DOI] |
| 10. | Castells A, Quintero E, Bujanda L, Castán-Cameo S, Cubiella J, Díaz-Tasende J, Lanas Á, Ono A, Serra-Burriel M, Frías-Arrocha E, Hernández C, Jover R, Andreu M, Carballo F, Morillas JD, Salas D, Almazán R, Alonso-Abreu I, Banales JM, Hernández V, Portillo I, Vanaclocha-Espí M, de la Vega M; COLONPREV study investigators. Effect of invitation to colonoscopy versus faecal immunochemical test screening on colorectal cancer mortality (COLONPREV): a pragmatic, randomised, controlled, non-inferiority trial. Lancet. 2025;405:1231-1239. [PubMed] [DOI] |
| 11. | Lișcu HD, Verga N, Atasiei DI, Badiu DC, Dumitru AV, Ultimescu F, Pavel C, Stefan RE, Manole DC, Ionescu AI. Biomarkers in Colorectal Cancer: Actual and Future Perspectives. Int J Mol Sci. 2024;25:11535. [PubMed] [DOI] |
| 12. | Imperiale TF, Ransohoff DF, Itzkowitz SH, Levin TR, Lavin P, Lidgard GP, Ahlquist DA, Berger BM. Multitarget stool DNA testing for colorectal-cancer screening. N Engl J Med. 2014;370:1287-1297. [PubMed] [DOI] |
| 13. | Imperiale TF, Porter K, Zella J, Gagrat ZD, Olson MC, Statz S, Garces J, Lavin PT, Aguilar H, Brinberg D, Berkelhammer C, Kisiel JB, Limburg PJ; BLUE-C Study Investigators. Next-Generation Multitarget Stool DNA Test for Colorectal Cancer Screening. N Engl J Med. 2024;390:984-993. [PubMed] [DOI] |
| 14. | Zeng T, Huang Z, Yu X, Zheng L, Liu T, Tian B, Xiao S, Huang J. Combining methylated SDC2 test in stool DNA, fecal immunochemical test, and tumor markers improves early detection of colorectal neoplasms. Front Oncol. 2023;13:1166796. [PubMed] [DOI] |
| 15. | Wang J, Liu S, Wang H, Zheng L, Zhou C, Li G, Huang R, Wang H, Li C, Fan X, Fu X, Wang X, Guo H, Guan J, Sun Y, Song X, Li Z, Mu D, Sun J, Liu X, Qi Y, Niu F, Chen C, Wu X, Wang X, Song X, Zou H. Robust performance of a novel stool DNA test of methylated SDC2 for colorectal cancer detection: a multicenter clinical study. Clin Epigenetics. 2020;12:162. [PubMed] [DOI] |
| 18. | 谭 能姣, 张 德庆. 粪便sdc2、tfpi2、sfrp2基因甲基化联合检测在结直肠癌早期筛查中的临床价值. 胃肠病学和肝病学杂志. 2023;32:847-851. [DOI] |
| 19. | Choi HI, Cha JM. Non-invasive colorectal cancer screening: emerging tools and clinical evidence. Clin Endosc. 2025. [PubMed] [DOI] |
| 20. | Órdenes P, Carril Pardo C, Elizondo-Vega R, Oyarce K. Current Research on Molecular Biomarkers for Colorectal Cancer in Stool Samples. Biology (Basel). 2023;13:15. [PubMed] [DOI] |
| 21. | Santos DAR, Gaiteiro C, Santos M, Santos L, Dinis-Ribeiro M, Lima L. MicroRNA Biomarkers as Promising Tools for Early Colorectal Cancer Screening-A Comprehensive Review. Int J Mol Sci. 2023;24:11023. [PubMed] [DOI] |
| 22. | Herring E, Tremblay É, McFadden N, Kanaoka S, Beaulieu JF. Multitarget Stool mRNA Test for Detecting Colorectal Cancer Lesions Including Advanced Adenomas. Cancers (Basel). 2021;13:1228. [PubMed] [DOI] |
| 23. | Bosch LJW, de Wit M, Pham TV, Coupé VMH, Hiemstra AC, Piersma SR, Oudgenoeg G, Scheffer GL, Mongera S, Sive Droste JT, Oort FA, van Turenhout ST, Larbi IB, Louwagie J, van Criekinge W, van der Hulst RWM, Mulder CJJ, Carvalho B, Fijneman RJA, Jimenez CR, Meijer GA. Novel Stool-Based Protein Biomarkers for Improved Colorectal Cancer Screening: A Case-Control Study. Ann Intern Med. 2017;167:855-866. [PubMed] [DOI] |
| 24. | Bond A, Greenwood R, Lewis S, Corfe B, Sarkar S, O'Toole P, Rooney P, Burkitt M, Hold G, Probert C. Volatile organic compounds emitted from faeces as a biomarker for colorectal cancer. Aliment Pharmacol Ther. 2019;49:1005-1012. [PubMed] [DOI] |
| 25. | Conde-Pérez K, Aja-Macaya P, Buetas E, Trigo-Tasende N, Nasser-Ali M, Rumbo-Feal S, Nión P, Arribas EM, Estévez LS, Otero-Alén B, Noguera JF, Concha Á, Pardiñas-López S, Carda-Diéguez M, Gómez-Randulfe I, Martínez-Lago N, Ladra S, Aparicio LMA, Bou G, Mira Á, Vallejo JA, Poza M. The multispecies microbial cluster of Fusobacterium, Parvimonas, Bacteroides and Faecalibacterium as a precision biomarker for colorectal cancer diagnosis. Mol Oncol. 2024;18:1093-1122. [PubMed] [DOI] |
| 26. | Heestermans R, Schots R, De Becker A, Van Riet I. Liquid Biopsies as Non-Invasive Tools for Mutation Profiling in Multiple Myeloma: Application Potential, Challenges, and Opportunities. Int J Mol Sci. 2024;25:5208. [PubMed] [DOI] |
| 28. | Lu DC, Zhang QF, Li L, Luo XK, Liang B, Lu YH, Hu BL, Jiang HX. Methylated Septin9 has moderate diagnostic value in colorectal cancer detection in Chinese population: a multicenter study. BMC Gastroenterol. 2022;22:232. [PubMed] [DOI] |
| 29. | Church TR, Wandell M, Lofton-Day C, Mongin SJ, Burger M, Payne SR, Castaños-Vélez E, Blumenstein BA, Rösch T, Osborn N, Snover D, Day RW, Ransohoff DF; PRESEPT Clinical Study Steering Committee, Investigators and Study Team. Prospective evaluation of methylated SEPT9 in plasma for detection of asymptomatic colorectal cancer. Gut. 2014;63:317-325. [PubMed] [DOI] |
| 30. | Jin P, Kang Q, Wang X, Yang L, Yu Y, Li N, He YQ, Han X, Hang J, Zhang J, Song L, Han Y, Sheng JQ. Performance of a second-generation methylated SEPT9 test in detecting colorectal neoplasm. J Gastroenterol Hepatol. 2015;30:830-833. [PubMed] [DOI] |
| 31. | Wang Z, He Z, Lin R, Feng Z, Li X, Sui X, Gu L, Xia T, Zhou D, Zhao B, Li Y, Li Z, Bai Y. Evaluation of a plasma cell-free DNA methylation test for colorectal cancer diagnosis: a multicenter clinical study. BMC Med. 2024;22:436. [PubMed] [DOI] |
| 32. | Gallardo-Gómez M, Rodríguez-Girondo M, Planell N, Moran S, Bujanda L, Etxart A, Castells A, Balaguer F, Jover R, Esteller M, Cubiella J, Gómez-Cabrero D, De Chiara L. Serum methylation of GALNT9, UPF3A, WARS, and LDB2 as noninvasive biomarkers for the early detection of colorectal cancer and advanced adenomas. Clin Epigenetics. 2023;15:157. [PubMed] [DOI] |
| 33. | Galoș D, Gorzo A, Balacescu O, Sur D. Clinical Applications of Liquid Biopsy in Colorectal Cancer Screening: Current Challenges and Future Perspectives. Cells. 2022;11:3493. [PubMed] [DOI] |
| 34. | Wu X, Zhang Y, Hu T, He X, Zou Y, Deng Q, Ke J, Lian L, He X, Zhao D, Cai X, Chen Z, Wu X, Fan JB, Gao F, Lan P. A novel cell-free DNA methylation-based model improves the early detection of colorectal cancer. Mol Oncol. 2021;15:2702-2714. [PubMed] [DOI] |
| 35. | Ganig N, Baenke F, Thepkaysone ML, Lin K, Rao VS, Wong FC, Polster H, Schneider M, Helm D, Pecqueux M, Seifert AM, Seifert L, Weitz J, Rahbari NN, Kahlert C. Proteomic Analyses of Fibroblast- and Serum-Derived Exosomes Identify QSOX1 as a Marker for Non-invasive Detection of Colorectal Cancer. Cancers (Basel). 2021;13:1351. [PubMed] [DOI] |
| 36. | 樊 建春, 曹 欣然, 杨 春白雪, 张 斌, 张 义炫, 夏 蕾, 武 雪亮. 基于蛋白质组学分析环形交叉轴突导向受体同源物4和原钙黏素12在结直肠癌中筛查、诊断和分期的临床意义. 中国医学科学院学报. 2025;47:910-920. [DOI] |
| 37. | Zhu M, Dang Y, Yang Z, Liu Y, Zhang L, Xu Y, Zhou W, Ji G. Comprehensive RNA Sequencing in Adenoma-Cancer Transition Identified Predictive Biomarkers and Therapeutic Targets of Human CRC. Mol Ther Nucleic Acids. 2020;20:25-33. [PubMed] [DOI] |
| 38. | Xu H, Wang C, Song H, Xu Y, Ji G. RNA-Seq profiling of circular RNAs in human colorectal Cancer liver metastasis and the potential biomarkers. Mol Cancer. 2019;18:8. [PubMed] [DOI] |
| 39. | Chen LJ, Chen X, Niu XH, Peng XF. LncRNAs in colorectal cancer: Biomarkers to therapeutic targets. Clin Chim Acta. 2023;543:117305. [PubMed] [DOI] |
| 40. | Deng L, Ismond K, Liu Z, Constable J, Wang H, Alatise OI, Weiser MR, Kingham TP, Chang D. Urinary Metabolomics to Identify a Unique Biomarker Panel for Detecting Colorectal Cancer: A Multicenter Study. Cancer Epidemiol Biomarkers Prev. 2019;28:1283-1291. [PubMed] [DOI] |
| 41. | Kim ER, Kwon HN, Nam H, Kim JJ, Park S, Kim YH. Urine-NMR metabolomics for screening of advanced colorectal adenoma and early stage colorectal cancer. Sci Rep. 2019;9:4786. [PubMed] [DOI] |
| 42. | Repici A, Badalamenti M, Maselli R, Correale L, Radaelli F, Rondonotti E, Ferrara E, Spadaccini M, Alkandari A, Fugazza A, Anderloni A, Galtieri PA, Pellegatta G, Carrara S, Di Leo M, Craviotto V, Lamonaca L, Lorenzetti R, Andrealli A, Antonelli G, Wallace M, Sharma P, Rosch T, Hassan C. Efficacy of Real-Time Computer-Aided Detection of Colorectal Neoplasia in a Randomized Trial. Gastroenterology. 2020;159:512-520.e7. [PubMed] [DOI] |
| 43. | Xu H, Tang RSY, Lam TYT, Zhao G, Lau JYW, Liu Y, Wu Q, Rong L, Xu W, Li X, Wong SH, Cai S, Wang J, Liu G, Ma T, Liang X, Mak JWY, Xu H, Yuan P, Cao T, Li F, Ye Z, Shutian Z, Sung JJY. Artificial Intelligence-Assisted Colonoscopy for Colorectal Cancer Screening: A Multicenter Randomized Controlled Trial. Clin Gastroenterol Hepatol. 2023;21:337-346.e3. [PubMed] [DOI] |
| 44. | Seager A, Sharp L, Neilson LJ, Brand A, Hampton JS, Lee TJW, Evans R, Vale L, Whelpton J, Bestwick N, Rees CJ; COLO-DETECT trial team. Polyp detection with colonoscopy assisted by the GI Genius artificial intelligence endoscopy module compared with standard colonoscopy in routine colonoscopy practice (COLO-DETECT): a multicentre, open-label, parallel-arm, pragmatic randomised controlled trial. Lancet Gastroenterol Hepatol. 2024;9:911-923. [PubMed] [DOI] |
| 45. | Xu X, Ba L, Lin L, Song Y, Zhao C, Yao S, Cao H, Chen X, Mu J, Yang L, Feng Y, Wang Y, Wang B, Zheng Z. Evaluation efficacy and accuracy of a real-time computer-aided polyp detection system during colonoscopy: a prospective, multicentric, randomized, parallel-controlled study trial. Surg Endosc. 2025;39:7417-7427. [PubMed] [DOI] |
| 46. | Wallace MB, Sharma P, Bhandari P, East J, Antonelli G, Lorenzetti R, Vieth M, Speranza I, Spadaccini M, Desai M, Lukens FJ, Babameto G, Batista D, Singh D, Palmer W, Ramirez F, Palmer R, Lunsford T, Ruff K, Bird-Liebermann E, Ciofoaia V, Arndtz S, Cangemi D, Puddick K, Derfus G, Johal AS, Barawi M, Longo L, Moro L, Repici A, Hassan C. Impact of Artificial Intelligence on Miss Rate of Colorectal Neoplasia. Gastroenterology. 2022;163:295-304.e5. [PubMed] [DOI] |
| 47. | Shung DL, Byrne MF. How Artificial Intelligence Will Impact Colonoscopy and Colorectal Screening. Gastrointest Endosc Clin N Am. 2020;30:585-595. [PubMed] [DOI] |
| 48. | Lui TKL, Lam CP, Tsui VW, Hui RW, To EW, Mak LL, Ko MK, Liu KS, Hui CK, Liu JJ, Xiao X, Leung WK. Prospective evaluation of artificial intelligence-assisted monitoring of the effective withdrawal time on adenoma detection. Intest Res. 2026. [PubMed] [DOI] |
| 49. | Liu X, Isa NAM, Chen C, Lv F. Colorectal Polyp Segmentation Based on Deep Learning Methods: A Systematic Review. J Imaging. 2025;11:293. [PubMed] [DOI] |
| 50. | Wang Z, Wang Z, Sun P. Deep learning model for gastrointestinal polyp segmentation. Peer J Comput Sci. 2025;11:e2924. [PubMed] [DOI] |
| 51. | Los B, Rocha BA, da Silva DN, Ribeiro VM, Kohara MA, Rodrigues RA, Pintão MCT, Pereira OJE, de Morais Malvezzi JV, da Silva FH, de Souza PHA, Araújo DC. AI-driven pre-screening for colorectal cancer using complete blood counts: toward broader population impact. Int J Colorectal Dis. 2025;40:235. [PubMed] [DOI] |
| 52. | Loaiza-Bonilla A, Leyfman Y, Cortiana V, Crawford R, Modi S. Defining a Multi-Omic, AI-Enabled Stool Screening Paradigm for Colorectal Cancer: A Consensus Framework for Clinical Translation. Cancers (Basel). 2026;18:909. [PubMed] [DOI] |
| 53. | Julbø FMI, Henriksen AL, Pradhan M, Lindstrøm EK, Kostolomov I, Oukrif D, van der Schee L, Isaksen MX, Manet A, Skrede OJ, De Raedt S, Liestøl K, Askautrud HA, Eide TJ, Holme Ø, Kerr DJ, Shepherd NA, Lacle MM, Novelli M, Hveem TS, Kleppe A. Reliable classification of polyps based on artificial intelligence: a development and validation study. EClinicalMedicine. 2026;93:103826. [PubMed] [DOI] |
| 54. | D'Aquila ML, Linhares SM, Schultz KS, Hughes ML, Mongiu AK. Computer-assisted detection of colorectal polyps: a narrative review of clinical utility, ongoing limitations, and opportunities for advancement. Transl Gastroenterol Hepatol. 2026;11:29. [PubMed] [DOI] |
| 55. | Mori Y, Kopylov U, Sinonquel P, Ebigbo A, Dekker E, De Groof AJ, Ahmad OF, Kader R, Saftoiu A, Schoon E, Mascagni P, Bhandari P, Hann A, Antonelli G, Iacucci M, Pech O, Dray X, Spadaccini M, Campion JR, Hassan C, Messmann H, Bisschops R, Fuccio L, Facciorusso A, Tham T; and the ESGE AI Curriculum advisory and voting group. Curriculum for safe and effective use of artificial intelligence in endoscopy: European Society of Gastrointestinal Endoscopy (ESGE) Position Statement. Endoscopy. 2026;58:202-210. [PubMed] [DOI] |
| 56. | Chen H, Lu B, Dai M. Colorectal Cancer Screening in China: Status, Challenges, and Prospects - China, 2022. China CDC Wkly. 2022;4:322-328. [PubMed] [DOI] |
| 57. | Ladabaum U, Mannalithara A, Meester RGS, Gupta S, Schoen RE. Cost-Effectiveness and National Effects of Initiating Colorectal Cancer Screening for Average-Risk Persons at Age 45 Years Instead of 50 Years. Gastroenterology. 2019;157:137-148. [PubMed] [DOI] |
| 58. | Levin TR, Corley DA, Jensen CD, Schottinger JE, Quinn VP, Zauber AG, Lee JK, Zhao WK, Udaltsova N, Ghai NR, Lee AT, Quesenberry CP, Fireman BH, Doubeni CA. Effects of Organized Colorectal Cancer Screening on Cancer Incidence and Mortality in a Large Community-Based Population. Gastroenterology. 2018;155:1383-1391.e5. [PubMed] [DOI] |
| 59. | Negoi I. Personalized surveillance in colorectal cancer: integrating circulating tumor DNA and artificial intelligence into post-treatment follow-up. World J Gastroenterol. 2025;31:106670. [PubMed] [DOI] |
| 60. | Liu J, Zhou R, Liu C, Liu H, Cui Z, Guo Z, Zhao W, Zhong X, Zhang X, Li J, Wang S, Xing L, Zhao Y, Ma R, Ni J, Li Z, Li Y, Zuo X. Automatic Quality Control System and Adenoma Detection Rates During Routine Colonoscopy: A Randomized Clinical Trial. JAMA Netw Open. 2025;8:e2457241. [PubMed] [DOI] |
| 61. | Brenner TA, Bujnak B, Alverson M, Strauss AT, Singh A, Ngamruengphong S, Khashab M, Singh V, Shin EJ, Akshintala VS. Development and Validation of an Automated, Real-time Adenoma Detection Rate and Colonoscopy Quality Metrics Calculator. Tech Innov Gastrointest Endosc. 2024;26:2-11. [PubMed] [DOI] |
学科分类: 胃肠病学和肝病学
手稿来源地: 陕西省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C, C
D级 (一般): 0
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁